Thèmes : médecine, sciences.
Conférence du mardi 15 avril 1986.
Le mardi 15 avril, Monsieur Milhaud, professeur de toxicologie à l’École Vétérinaire de Maisons-Alfort, est venu nous parler du fluor.
ÉVOLUTION DE LA TOXICOLOGIE.
La toxicologie est une science qui a beaucoup évolué depuis les dernières années. Il y a un siècle, c’était la science des poisons.
Ces derniers temps, la toxicologie a pris une nouvelle dimension. Elle est davantage destinée à protéger le public et l’environnement qu’à faire la preuve de quelques intoxications aigües exceptionnelles. On est ainsi passé de l’étude des intoxications aigües à l’étude de troubles qui peuvent se produire lorsqu’on ingère des petites quantités de substances toxiques pendant des périodes prolongées.
Toute une méthodologie s’est mise en place pour savoir comment on peut protéger le consommateur des substances nocives qui pourraient se trouver en quantité dangereuse dans l’alimentation.
LE FLUOR.
Le fluor (19F) est un élément relativement abondant du règne minéral. C’est un halogène comme le chlore, le brome, l’iode, qui, par suite de sa très grande réactivité, n’existe que tout à fait exceptionnellement dans la nature sous forme de gaz à l’état libre (F2). On l’y trouve donc pratiquement sous forme de dérivés minéraux (fluorures, fluosilicates, fluorophosphates, par exemple). L’appellation « fluor » pour l’ensemble de tous ces dérivés, naturels ou synthétiques, est tout à fait impropre. Il serait tout aussi aberrant de parler de l’action du chlore pour des dérivés aussi divers que le chlore gazeux, le chlorure de sodium, etc.
Dans la suite de l’exposé lorsque l’on parlera de fluor, on parlera en vérité de fluorure.
Les propriétés du fluor dépendent de la quantité ingérée.
En faible dose, le fluor se comporte comme un oligo-élément*.
* Elément minéral, métalloïdique ou métallique, présent dans l’organisme en très petites quantités. Certains de ces éléments jouent un rôle important dans les processus enzymatiques qui sont à la base du métabolisme cellulaire. Ils sont nécessaires à l’état de traces dans l’alimentation et leur carence peut se traduire par des troubles de ce métabolisme.
En dose plus élevée, il a des propriétés médicamenteuses.
En dose encore plus élevée, la substance peut devenir dangereuse.
Le fluor est présent dans notre environnement, dans le sol, dans les minerais, dans l’eau de boisson…
C’est l’eau qui intervient essentiellement dans l’apport alimentaire du fluor.
Les teneurs des eaux naturelles sont très variables.
Elles peuvent aller d’un dixième de mg/litre à une centaine de mg/litre. En France, les eaux sont considérées comme relativement pauvres en fluor puisqu’elles ont des teneurs qui se situent entre 0,1 mg/litre et 0,5 mg/litre. En Inde, en Islande, etc. les eaux sont très riches en fluor. C’est un danger potentiel pour la population car elles peuvent provoquer de la fluorose humaine et animale.
Rôle bénéfique.
Le fluorure de sodium qui se trouve dans l’eau est absorbé dans le tube digestif passe dans le sang.
Il a une affinité particulière pour les os et les dents. L’ion fluor F+ vient s’inclure dans les réseaux cristallins de phosphate tricalcique.
Il y a une teneur maximale de fluor dans l’os et dans la dent qui donne à la dent la plus grande résistance possible.
En France, les eaux de boisson sont pauvres en fluor et notre squelette et nos dents sont déficitaires en fluor. Cela n’a pas d’incidence sur le squelette, par contre, cela en a sur les dents.
La carie dentaire est un phénomène bactérien entrainant une désagrégation de la dent. Un trou se forme progressivement dans celle-ci. La carie progressera en fonction de la résistance de la dent et en fonction des attaques extérieures.
On sait maintenant que la meilleure qualité d’émail que l’on puisse avoir est celle obtenue lorsque les enfants boivent une eau contenant environ 1 mg/litre de fluor.
Dans certaines villes américaines, on a ajouté du fluor dans l’eau. Cela a inquiété un certain nombre de chercheurs. Des études épidémiologiques ont été effectuées. Dans les villes où l’on a entrepris ces études, on a noté qu’en même temps que l’on avait augmenté la teneur en fluor de l’eau, le pourcentage des enfants mongoliens avait augmenté. Mais y avait-il un lien entre les 2 affaires ? Les partisans de l’action bénéfique du fluor dans l’eau disaient qu’il n’y en avait aucun.
Au contraire, les autres prétendaient que tant que l’on n’avait pas démontré que le fluor n’avait pas provoqué ces accidents, le fluor ne devait pas être ajouté l’eau de boisson.
Il a fallu 25 ans pour que l’on démontre qu’il n’y avait pas de lien entre les 2 phénomènes.
Des dentifrices au fluor sont vendus ainsi que des chewing-gums. L’action du fluor dans un dentifrice n’est pas le même qu’une eau de boisson. Le fluor est surtout utilisé chez l’enfant avant que toute sa dentition ne soit établie. Le dentifrice est recraché, on n’avale donc pas le fluor qui s’y trouve. Le fluor a alors une action locale et non générale et n’est pas un moyen de protection suffisant pour l’enfant.
Le rôle du fluor dans l’eau n’est donc pas le même que celui dans le dentifrice.
Effets néfastes du fluor.
Le fluor à dose trop importante devient dangereux pour l’homme et pour les animaux. Il y a 2 grandes circonstances dans lesquelles la fluorose, c’est-à-dire l’intoxication par le fluor apparaît :
- lorsqu’il y a un excès de fluor dans le sol,
- lorsqu’on se trouve au voisinage d’industries qui ont des effluents trop riches en fluor.
Monsieur Milhaud nous a montré de nombreuses diapositives illustrant ces propos.
Tout d’abord une oasis en Tunisie renfermant des sources contenant des teneurs de 2 à 5 mg/l de fluor.
Les dents des enfants sont colorées et déformées.
Cela est dû à la fois à l’eau et à la consommation élevée de dattes.
Une autre diapositive nous montre une mine de phosphate ciel ouvert, toujours en Tunisie. Les moutons qui se nourrissent aux alentours ont un double apport fluoré : par les plantes et par la poussière.
Dans l’usine qui traite le phosphate dans ce même pays, on fabrique des engrais. Pour cette opération, on ajoute sur les phosphates de l’acide sulfurique. Il se dégage de l’acide fluorhydrique gazeux, soluble dans l’eau. On retrouve le fluor dans les déchets de l’usine, qui sont rejetés dans la mer. Le golfe de Gabès est ainsi contaminé. Cela a un effet sur la population qui vit dans ce golfe (par l’intermédiaire entre autres des poissons).
En France, il existe dans certains sites, une fluorose dite industrielle. Ce sont surtout les usines d’aluminium qui provoquent cet excès de fluor.
La fabrication de l’aluminium par l’électrolyse de l’alumine en présence de cryolithe provoque l’émission d’acide fluorhydrique à l’état gazeux et de particules, dont certaines sont très fines et contiennent de la cryolithe, du fluorure d’aluminium, du fluorure de calcium et de la chiolite (Na5Al3F14).
La dispersion et la retombée des composés émis dans l’atmosphère dépendent du relief, des conditions climatiques et atmosphériques et de leur état physique (gazeux, en solution, …).
Les dérivés fluorés contenus dans l’atmosphère pénètrent directement dans les feuilles de végétaux par les stomates (voir conférence sur les pluies acides). On a ainsi une pollution des pâturages et des potagers. Les bovins et les moutons ingèrent une grande quantité d’herbe par jour. Les hommes eux mangent des légumes en faible quantité qui, de plus, sont lavés. Autour de ces usines, la pollution n’a pas atteint des taux toxiques pour l’homme mais seulement pour les animaux.
Les animaux domestiques chez lesquels on rencontre de la fluorose peuvent être classés comme suit par ordre de sensibilité décroissante :
- jeunes bovins,
- jeunes ovins et caprins,
- vaches laitières,
- brebis et chèvres
- bovins à l’engrais,
- – chevaux.
Monsieur Milhaud nous montre les usines d’aluminium de Lannemezan, de St Jean de Maurienne, de Noguères.
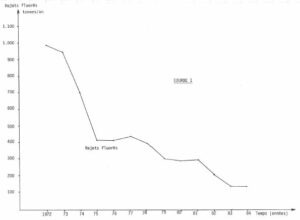
De nouvelles usines remplacent maintenant les anciennes. Elles permettent une diminution notable de la pollution. Sur la courbe 1 on voit qu’en 1976, les rejets fluorés étaient de 400 tonnes par an. Elles atteignent en 1984 150 tonnes par an.
La première manifestation de fluorose est constituée par une légère modification de l’émail des incisives qui devient opaque, crayeux, marbré.
La gravité de la lésion dentaire dépend de la quantité de fluor ingéré pendant que la dent se forme.
PRÉVENTION ET TRAITEMENT DE LA FLUOROSE CHEZ LES ANIMAUX.
Le traitement de la fluorose étant pratiquement inexistant, tout l’effort doit porter sur la prévention.
On peut tout d’abord prendre des dispositions pour diminuer l’apport alimentaire du fluor d’une part en n’utilisant que des phosphates défluorés pour l’alimentation des animaux, d’autre part en dotant les installations industrielles de dispositifs de captation efficace. Il peut être intéressant de mettre en place un système de contrôle périodique et systématique de la contamination de l’alimentation, afin de retirer les aliments trop fortement contaminés et de les remplacer par des aliments sains.
De nombreux procédés ont été expérimentés pour diminuer l’absorption intestinale de fluor en ayant recours aux sels de calcium ou d’aluminium.
Ce qu’il convient de noter, c’est la faible marge entre les doses ayant des effets bénéfiques sur ce grand problème sanitaire et économique que constituent la carie dentaire et les premiers symptômes de fluorose.
L’utilisation de dérivés fluorés aussi bien à petites doses, surtout pendant la période de formation des dents pour assurer une bonne prévention de la carie dentaire, qu’à doses plus fortes dans des cas très particuliers (ostéoporose, …) doit donc être ponctuelle, convenablement évaluée et contrôlée, de préférence sous contrôle médicale.
ANNEXE 1
ANALYSES MINÉRALES
EAUX MINÉRALES : RÉSULTATS DES ANALYSES
| MARQUE | MINÉRALISATION | DURETÉ | FLUOR |
|
(mg/l) |
(mg/l) | ||
| APOLINARIS | Forte | Dure | 0.6 |
| APLINE | Moyenne | Dure | 1.2 |
| BADOIT | Moyenne | Dure | 1.2 |
| CONTREXEVILLE | Forte | Très dure | 0.3 |
| COUZAN BRAULT | Forte | Dure | 2.3 |
| EVIAN | Faible | Dure | 0.1 |
| PERRIER | Faibl e | Dure | 0. 2 |
| PIERVAL | Faible | Dure | 0.2 |
| ROCHE SANTEUIL | Faible | Dure | 0.4 |
| ROXANE | Très faible | Très douce | 0.1 |
| VALS FAVORITE | Forte | Dure | 1.9 |
| VENUS | Faible | Dure | 0.3 |
| VICHY Célestins | Très forte | Dure | 5.4 |
| VICHY St-Yorre | Très forte | Dure | 7.9 |
| VITTEL, Grande source | Moyenne | Dure | 0.5 |
| VITTEL Hépar | Forte | Très dure | 0.5 |
| VITTELLOISE | Faible | Dure | 0.2 |
| VOLVIC | Très faible | Très douce | 0.4 |
ANNEXE II
UTILISATIONS DU FLUOR ET DE SES DÉRIVÉS
La principale application du fluor qui est d’ailleurs à l’origine de son développement industriel durant la IIe guerre mondiale, est la fabrication de l’hexafluorure d’uranium destiné à la séparation des isotopes de l’uranium.
Le secteur nucléaire lui offre un second débouché avec le retraitement, par procédés de voie sèche, des combustibles sortant des réacteurs. La volatilisation des hexafluorures permet en effet la séparation des produits issus de la fission, la récupération du plutonium et le recyclage de l’uranium.
La préparation des fluorures d’halogène (CLF3, CLF5, B2F3, B2F5, IF5, FF7), de l’hexafluorure de soufre SF6 fait également appel au fluor (l’hexafluorure de soufre est employé isolant en électricité). Il en est de même des hexafluorures de métaux réfractaires : molybdène, tungstène.
Citons aussi l’emploi du fluor liquide comme propergol pour la propulsion des fusées et missiles.
Indispensable à la préparation d’autres propergols fluorés, tels que les fluorures de chlore, d’oxygène, la tétrafluorhydrazine, le fluor peut encore trouver, sous cette forme, une autre application dans le domaine spatial.
Certains fluorocarbones sont des agents de transfert de chaleur. Beaucoup sont utilisés en électronique. Les fluorocarbones polyhalogénés (fréons, halons, …) sont utilisés comme solvants, réfrigérants, pulseurs, extincteurs.
Plusieurs matières plastiques sont dérivées du tétrafluoroéthylène. Divers élastomères sont de plus en plus utilisés.
L’acide fluorhydrique (HF) est utilisé pour la gravure sur verre, comme agent de nettoyage et de décapage, comme catalyseur, pour la fabrication des fluorures et enfin pour l’alcoylation de l’essence pour préparer des hydrocarbures à haut pouvoir antidétonnant.
Découvrez + de 1100 textes des conférences du CDI sur le site du CDI de Garches
Vos commentaires et vos conseils contribuent à l’amélioration de nos parutions.
Vous disposez de l’espace « COMMENTAIRES » ci-dessous pour les exprimer.
Merci et à bientôt pour votre prochaine visite.

Laisser un commentaire