Thèmes: Médecine, Sciences
Conférence du mardi 17 mars 2026
Par le Professeur Erwan POUPON, Professeur des universités — Faculté de Pharmacie, Université Paris-Saclay, Laboratoire BiOCIS (CNRS) — Pharmacognosie & Chimie des substances naturelles
Une histoire de substances naturelles marines
PLAN
1. Le médicament : du principe actif au marché
2. Les substances naturelles : définition et rôles biologiques
3. Les sciences « omiques » : outils modernes de la recherche
4. L’océan comme source de biodiversité et de chimiodiversité
5. Les médicaments marins : un panorama de la quinzaine de spécialités commercialisées
6. Les conjugués anticorps-cytotoxines : la révolution des ADC
7. Défis de production, enjeux éthiques et perspectives d’avenir
8. Questions/réponses : sujets complémentaires abordés

- 1. Le médicament : du principe actif au marché
- 1.1 Définition et composantes
Un médicament, dit de « spécialité », ne se résume pas à son principe actif (ex. paracétamol dans Dafalgan®). Il comprend également des excipients (véhicule, stabilisants, arômes…) et une forme galénique adaptée (comprimé, gélule, préparations injectables, crème…). L’ensemble de ces éléments relève d’un véritable « art pharmaceutique » intégrant un nombre croissant de technologies.
Le principe actif est identifié par sa Dénomination Commune Internationale (DCI), nom universel utilisé par l’ensemble des professionnels de santé à travers le monde, indépendamment du nom de marque déposé par le laboratoire.
-
- 1.2 Un développement long et coûteux
La mise au point d’un médicament requiert en moyenne 10 à 20 ans entre la découverte de la molécule et son autorisation de mise sur le marché (AMM). L’AMM, délivrée par les autorités de santé, garantit la sécurité, l’efficacité et la qualité du médicament avant toute commercialisation.
| Règle des 10 000 : sur 10 000 molécules candidates issues des laboratoires de recherche, une seule parviendra sur le marché. Ce taux d’attrition considérable explique un coût moyen de développement estimé à 1 milliard d’euros minimum, pouvant dépasser 2,5 milliards de dollars pour les molécules les plus complexes.
Conséquence : seul un médicament sur dix est réellement rentable. L’industrie pharmaceutique est donc celle qui réinvestit proportionnellement le plus en R&D. |
|---|
-
- 1.3 Des acteurs en mutation : « Big Pharma » vs. « Biotech »
Historiquement, les grands groupes pharmaceutiques (Sanofi, Pfizer, Roche…) assuraient l’intégralité du cycle de vie du médicament. Depuis les années 2000, on observe un transfert majeur de la R&D vers des entreprises de biotechnologie (biotech) de plus petite taille, plus agiles et spécialisées.
Aux États-Unis, plus de 60 % des médicaments qui arrivent sur le marché ont été découverts dans des « biotech ». Les « Big Pharma » achètent ces entreprises ou co-développent les molécules prometteuses souvent désormais au stade des essais chez l’Humain, ayant elles-mêmes réduit leurs activités de recherche fondamentale.
-
- 1.4 Brevets, génériques et cycle de vie
Un brevet pharmaceutique dure environ 20 ans. À son expiration, d’autres industriels peuvent commercialiser un médicament générique contenant le même principe actif, aux mêmes doses, mais à un coût de production bien inférieur. Le générique doit démontrer sa bioéquivalence par rapport au médicament princeps. Dans la très grande majorité des cas, il ne présente aucune différence clinique significative.
Pour des informations sur le cycle de vie du médicament : le site du leem.
- 2. Les substances naturelles : définition et rôles biologiques
- 2.1 Une définition centrée sur le métabolisme
● Les substances naturelles sont des petites molécules organiques produites par des êtres vivants. Elles appartiennent au métabolisme dit « secondaire » ou « spécialisé », par opposition au métabolisme « primaire » universel qui correspond à la biochimie assurant la vie des êtres vivants et essentiellement tourné vers la production d’énergie. Ce métabolisme « secondaire » n’est pas partagé par tous les organismes : il est propre à certaines espèces, voire à une seule.
●Exemples emblématiques : seul le pavot somnifère (Papaver somniferum) produit la morphine ; seul les quinquinas (Cinchona sp.) produisent la quinine ; seule la pervenche tropicale (Catharanthus roseus) biosynthétise la vinblastine.
-
- 2.2 Endo- et exométabolites
On distingue deux catégories fonctionnelles :
- Les « endométabolites » : molécules régulatrices internes (progestérone, testostérone, adrénaline, sérotonine, insuline…). Tous les êtres vivants produisent ce type de substances qui assurent leur « homéostasie ».
- Les « exométabolites » : molécules libérées dans l’environnement, jouant un rôle de communication (phéromones chez les insectes sociaux) ou de défense (antibiotiques naturels, toxines végétales).
Principe fondamental : les molécules naturelles utilisées comme anticancéreux ou antibiotiques n’ont pas été « conçues » pour soigner l’Homme ! Elles résultent de l’évolution et servent les organismes qui les produisent (défense contre les prédateurs, compétition avec d’autres espèces, etc.). La recherche pharmaceutique détourne ainsi à son profit des arsenaux chimiques façonnés sur des millions d’années.
-
- 2.3 Des molécules historiques issues des plantes
La pharmacognosie (étude des médicaments d’origine naturelle) a d’abord exploité les plantes médicinales. Parmi les grandes molécules végétales qui ont marqué l’histoire de la pharmacie :
- Morphine (pavot) — analgésique majeur de référence
- Quinine (quinquina) — antipaludique historique
- Paclitaxel / Taxol® (if du Pacifique) — anticancéreux majeur
- Vinblastine / Vincristine (pervenche de Madagascar) — anticancéreux
- Artémisinine (armoise annuelle) — antipaludique issu de la médecine traditionnelle chinoise, Prix Nobel de médecine 2015
- Nicotine (tabac) — utilisée en substitution nicotinique
Un article récent sur les médicaments d’origine naturelle : cliquez.
Ces molécules végétales ont ouvert la voie, mais le Pr Poupon souligne que les micro-organismes (bactéries, champignons, cyanobactéries) constituent désormais un terrain bien plus fertile pour la découverte de nouvelles molécules, notamment les micro-organismes marins.
- 3. Les sciences « omiques » : outils modernes de la recherche
- 3.1 Le génome, le protéome, le métabolome
Les « sciences omiques » désignent l’ensemble des approches globales permettant d’étudier simultanément l’intégralité des molécules d’un type donné dans un organisme :
- Génomique : séquençage partiel ou complet de l’ADN d’un organisme vivant, identification des gènes codant pour des protéines (enzymes biosynthétiques d’intérêt par exemple).
- Transcriptomique : analyse et séquençage des ARN messagers (reflet des gènes qui s’expriment à un temps t).
- Protéomique : caractérisation de l’ensemble des protéines exprimées à un temps t (structure, interactions, fonctions).
- Métabolomique : analyse du métabolome, c’est-à-dire de l’ensemble des petites molécules (métabolites) présentes dans un organisme ou un échantillon à un temps t.
Ces approches ont révolutionné la recherche en substances naturelles depuis 20-25 ans, permettant de passer d’une exploration molécule par molécule à une vision systémique du vivant à l’heure des sciences des données (« big data »).
-
- 3.2 AlphaFold et l’intelligence artificielle
Un tournant majeur a été la mise au point d’AlphaFold, outil d’intelligence artificielle développé par DeepMind (Alphabet/Google : https://alphafold.ebi.ac.uk/ ), qui prédit avec une très haute précision la structure tridimensionnelle des protéines. Là où des décennies de cristallographie auraient été nécessaires, AlphaFold peut analyser des millions de protéines en quelques semaines.
| Les créateurs d’AlphaFold ont reçu le Prix Nobel de Chimie 2024, fait exceptionnel pour des travaux réalisés par de jeunes chercheurs issus d’une entreprise technologique. Ce Nobel illustre la convergence entre informatique, IA et sciences du vivant. |
|---|
-
- 3.3 La métabolomique au laboratoire du Pr Poupon
Le laboratoire BioCIS développe des outils de métabolomique avancés, combinant chromatographie liquide haute performance (HPLC) et spectrométrie de masse (MS). Cette approche permet d’identifier des centaines de métabolites dans un seul échantillon complexe, y compris des molécules présentes en très faibles quantités. Ces approches accélère grandement le processus de découvertes de nouvelles substances naturelles et évitent d’isoler des composés déjà connus.
Ces analyses sont aujourd’hui dopées à l’IA : de nombreux logiciels « open-source », accessibles gratuitement pour la recherche académique, permettent le traitement automatisé de quantités de données chromatographiques massives.
-
- 3.4 La génomique comme boussole pour la découverte
Une approche émergente consiste à séquencer d’abord le génome d’un micro-organisme (de l’environnement marin par exemple) pour identifier ses clusters de gènes biosynthétiques (« BGC »), puis à faire exprimer ces gènes dans un organisme hôte facilement cultivable (ex. E. coli). Cette stratégie de « genome mining » permet de découvrir des molécules que l’organisme source ne produit qu’en conditions particulières — voire pas du tout en culture standard.
- 4. L’océan, source de biodiversité et de chimiodiversité
- 4.1 Un milieu longtemps ignoré
Les océans couvrent plus de 70 % de la surface terrestre et hébergent une biodiversité immense, encore très largement inexplorée. Pourtant, la mer a longtemps inspiré la crainte (naufrages, expéditions perdues) et les traditions d’utilisation médicale des produits marins sont quasi-inexistantes en Europe, contrairement au Japon ou à d’autres cultures asiatiques.
La « bioprospection » marine n’a réellement débuté qu’à partir des années 1960, rendue possible par les scaphandres autonomes (brevets Cousteau-Gagnan, années 1940). Les premiers médicaments d’origine marine n’ont été commercialisés que dans les années 2000.
-
- 4.2 Des écosystèmes extrêmes, source de molécules inédites
Les conditions extrêmes des milieux marins (pression, obscurité, température quasi constante en profondeur, haute salinité) ont sélectionné des adaptations biochimiques uniques. Exemples d’ écosystèmes explorés :
- Récifs coralliens (eaux peu profondes, zone tropicale) : grande densité de biodiversité, riches en invertébrés (éponges, coraux, mollusques, tuniciers).
- Zones mésopélagiques (200 à 1000 m) : milieu aphotique, forte pression, organismes bioluminescents.
- Fentes hydrothermales (1000 m et plus) : températures pouvant dépasser 300°C à l’émission, organismes chimio-autotrophes totalement indépendants de la photosynthèse.
- Grands fonds (abysses, fosses océaniques) : pression extrême (600 bars à 6 000 m), température stable proche de 0°C.
- 4.3 Les micro-organismes marins, cœur de la richesse chimique
Contrairement à ce que l’on pourrait croire, la plupart des molécules actives trouvées dans des invertébrés marins (éponges, coraux, mollusques) ne sont pas produites par ces organismes eux-mêmes, mais par des micro-organismes (bactéries, cyanobactéries, champignons) vivant en symbiose avec eux. Cette découverte est fondamentale car elle oriente la recherche vers l’étude du microbiome associé à ces organismes. Elle n’est cependant pas toujours généralisable et des organismes marins peuvent produire des molécules originales « par eux-mêmes ».
| Les missions TARA Océans (en cours) ont collecté des milliers d’échantillons de plancton et de micro-organismes marins. Ces collections représentent plusieurs décennies de travail potentiel pour les chercheurs en chimie des substances naturelles marines. |
|---|
- 5. Les médicaments d’origine marine commercialisés : un panorama
Une quinzaine de médicaments d’origine marine sont à ce jour commercialisés en Europe et/ou aux États-Unis. Le Pr Poupon en présente les plus emblématiques, illustrant les différentes stratégies de développement.
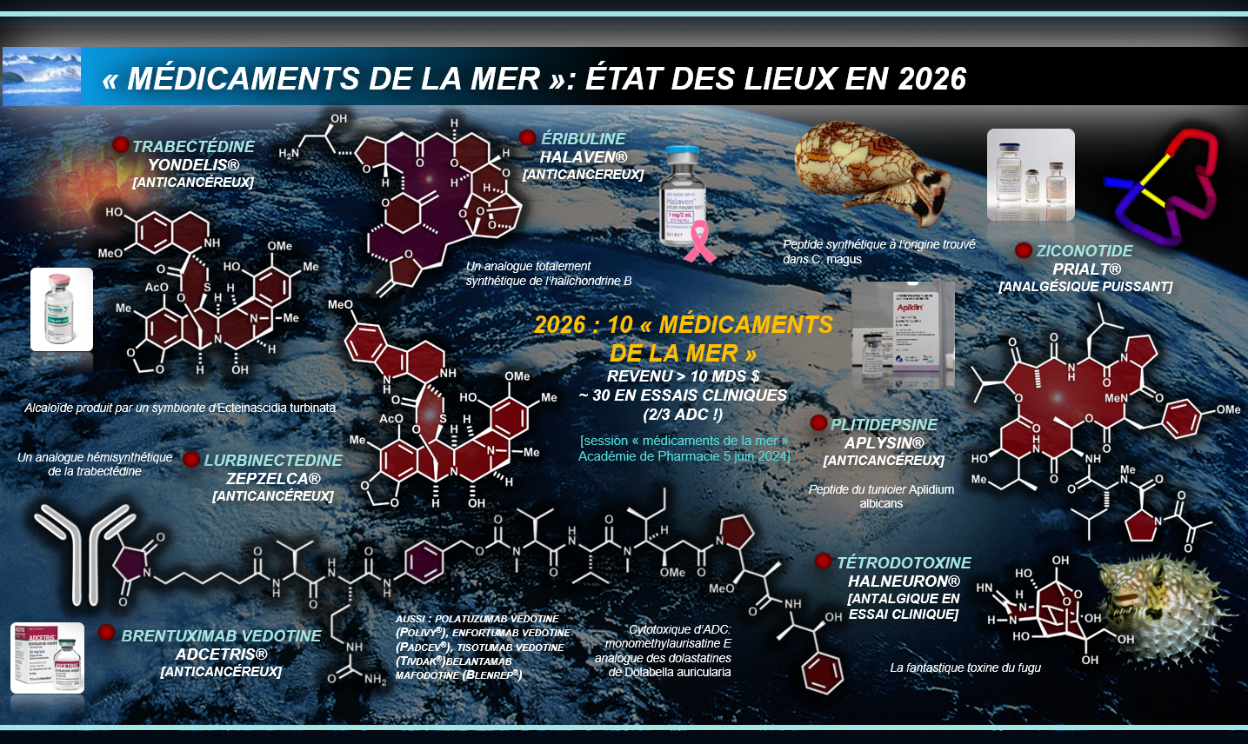
-
- 5.1 Le ziconotide (Prialt®) — analgésique issu d’un cône du Pacifique
Les cônes du Pacifique (« escargots de mer » dont la piqûre peut être mortelle) produisent des venins complexes contenant à la fois des peptides hautement toxiques et chez certaines espèces des peptides analgésiques. Le ziconotide, petit peptide isolé de ce venin, est un analgésique puissant utilisé en dernier recours dans des douleurs chroniques rebelles (cancer en phase terminale), administré par voie intrathécale. Son étude s’inscrit dans l’essor de la vénomique, discipline consacrée à l’analyse des molécules actives des venins et qui suscite un regain d’intérêt depuis une vingtaine d’années.
-
- 5.2 L’éribuline (Halaven®) — anticancéreux issu d’une éponge japonaise
L’éribuline est l’un des exemples les plus marquants de la complexité du développement d’un médicament marin. Elle dérive de l’halichondrine B, molécule naturelle isolée d’une éponge (Halichondria okadai) au large du Japon — la molécule étant en réalité produite par un micro-organisme symbionte. L’histoire comporte trois épisodes clés :
- Isolement : 2 tonnes d’éponges ont été nécessaires pour obtenir quelques dizaines de milligrammes d’halichondrine B, quantité suffisante pour déterminer sa structure et démontrer son activité.
- Simplification structurale : seule une partie de la molécule naturelle concentre toute l’activité anticancéreuse (inhibition de la polymérisation de la tubuline, même mécanisme que la vinblastine d’origine végétale). L’éribuline commercialisée est un analogue synthétique correspondant à cette partie de la molécule suffisante à l’activité.
- Synthèse totale : l’éribuline est produite par synthèse chimique en 60 étapes, faisant d’elle la molécule la plus complexe issue de l’industrie de la chimie fine. Des génériques viennent de faire leur entrée sur le marché.
- 1.5.3 La trabectédine (Yondelis®) — anticancéreux européen issu d’un tunicier
La trabectédine est commercialisée par la société espagnole PharmaMar, spécialisée dans les médicaments d’origine marine. Elle a été découverte dans un tunicier (Ecteinascidia turbinata), invertébré proche des vertébrés sur le plan évolutif, présent en Méditerranée et dans les Caraïbes. La production industrielle repose sur l’hémisynthèse : une molécule bactérienne structurellement proche (la cyanosafracine) est produite par fermentation puis modifiée chimiquement en 20 étapes pour donner la trabectédine. Bien que d’utilisation limitée (forte hépatotoxicité), ce médicament illustre l’importance de la chimie de synthèse pour surmonter les obstacles de production de molécules présentes en très faibles quantité. Le développement clinique de la trabectédine avait, tout de même, pu être fait avec la molécule extraite de sa source naturelle !
- 6. La révolution des conjugués anticorps-cytotoxiques (ADC)
- 6.1 Principe et enjeu
Les conjugués anticorps-agents cytotoxiques (Antibody-Drug Conjugates, ADC) représentent actuellement la part la plus importante du chiffre d’affaires des médicaments d’origine marine (plus de 10 milliards de dollars). Ils incarnent une double révolution thérapeutique.
Le principe de conception repose sur la combinaison de deux technologies :
- Un anticorps monoclonal, dirigé contre un antigène spécifiquement exprimé à la surface des cellules cancéreuses (ciblage de précision).
- Une molécule cytotoxique (souvent d’origine naturelle marine) greffée sur cet anticorps via un bras chimique (linker).
- 6.2 La stratégie du « cheval de Troie »
Une fois l’anticorps fixé sur sa cible tumorale, l’ensemble du complexe est internalisé par la cellule cancéreuse. L’anticorps est alors dégradé, libérant la molécule cytotoxique directement à l’intérieur de la cellule, où elle exerce son effet létal avec une précision et une efficacité qui se veulent bien supérieures à une chimiothérapie classique avec moins d’effets secondaires « collatéraux ».
| Une quinzaine d’ADC sont disponibles sur le marché européen, dont une dizaine en France. Ces médicaments sont très coûteux (plusieurs dizaines de milliers d’euros par traitement en France, jusqu’à 200 000 – 300 000 dollars aux États-Unis), en raison de la haute complexité des technologies mises en œuvre. |
|---|
-
- 6.3 Le rôle des molécules marines comme charges cytotoxiques
Dans plusieurs ADC commercialisés, la charge cytotoxique est d’origine marine. C’est notamment le cas des auristatines (védotine, monométhylauristatine E), petits peptides dérivés des dolastatines, elles-mêmes isolées du « lièvre de mer » (Dolabella auricularia) – un gastéropode sans coquille présent dans les eaux de La Réunion et du Pacifique. Les dolastatines sont en réalité produites par des cyanobactéries ingérées par ce mollusque.
Ces molécules, d’une toxicité cellulaire extrême mais facilement synthétisables (structure peptidique), agissent sur la tubuline – le même mécanisme que la vinblastine d’origine végétale (cf. conférence du Pr Guy Lewin) – ce qui illustre la convergence évolutive frappante entre organismes marins et terrestres.
-
- 6.4 Complexité technologique et enjeux industriels
Maîtriser un ADC implique simultanément : la production de l’anticorps monoclonal (bioréacteurs, purification), la synthèse du cytotoxique, la chimie de conjugaison (« linker »), le contrôle qualité de chacun de ces composants et leur assemblage final. Cette accumulation de technologies explique le coût élevé de ces thérapies et les enjeux croissants autour de leur accessibilité dans les systèmes de santé.
- 7. Défis de production, enjeux éthiques et perspectives d’avenir des médicaments « de la mer »
- 7.1 Les obstacles à la production industrielle
La valorisation des ressources marines soulève des défis de production considérables. Plusieurs solutions ont été explorées ou sont en cours de développement :
- Synthèse totale : solution ultime mais coûteuse (jusqu’à 60 étapes pour l’éribuline). Réservée aux molécules dont l’activité justifie l’investissement.
- Hémisynthèse : modification chimique d’une molécule naturelle proche, produite par fermentation. Cas de la trabectédine.
- Aquaculture d’invertébrés marins : techniquement possible mais jamais industrialisable de façon durable (fragilité des éponges, coraux, tuniciers face aux variations environnementales).
- Fermentation bactérienne : isoler et cultiver la bactérie symbiotique en dehors de l’organisme hôte. Souvent impossible dans les conditions actuelles.
- Génie génétique (solution d’avenir) : transférer les gènes biosynthétiques d’intérêt dans des bactéries facilement cultivables (E. coli, Streptomyces).
- 7.2 Enjeux éthiques et légaux : la Convention de Nagoya
L’exploitation des ressources biologiques marines soulève d’importantes questions de souveraineté et d’équité. La Convention de Nagoya (2010, entrée en vigueur 2014), dans le cadre de la Convention sur la diversité biologique (CDB), encadre l’accès aux ressources génétiques et impose un partage juste et équitable des avantages (bénéfices financiers, transfert de technologies) entre les États fournisseurs de biodiversité et les utilisateurs (industriels, chercheurs).
Le Pr Poupon soulève la question complexe du droit de propriété sur les ressources biologiques prélevées dans les eaux internationales : à qui appartient une molécule découverte au fond des océans, au-delà des zones économiques exclusives ?
-
- 7.3 Perspectives : vers une pharmacie marine du futur
Le Pr Poupon identifie plusieurs axes d’avenir :
- « Genome mining » : identifier les potentialités biosynthétiques de micro-organismes marins par séquençage à haut débit, avant même de cultiver les organismes.
- Repositionnement de molécules existantes (« drug repurposing ») : tester des molécules marines connues dans de nouvelles indications thérapeutiques.
- IA et modélisation moléculaire : prédire l’activité biologique de nouvelles molécules et accélérer les phases de criblage.
- Expéditions scientifiques en cours (Antarctique, suite de TARA) : des invertébrés inconnus continuent d’être découverts dans des environnements polaires, représentant une réserve potentielle de nouvelles molécules actives.
| Vision du Pr Poupon : « Nous allons étudier les génomes avant d’étudier les produits. » L’avenir de la pharmacie marine repose sur la biologie computationnelle et le génie génétique, permettant d’exploiter la richesse chimique des fonds marins sans prélèvement massif d’organismes vulnérables. |
|---|
-
- 7.4 Questions/réponses : thèmes complémentaires abordés
La session de questions a permis d’aborder plusieurs sujets connexes :
- Microbiote intestinal : le Pr Poupon insiste sur l’importance de prendre soin de son microbiote (alimentation, enjeux autour du « jeûne intermittent ») comme acte de prévention majeur.
- « Vénomique » : les venins d’animaux marins (cônes, oursins) et terrestres (araignées, scorpions, serpents) suscitent un regain d’intérêt grâce aux nouvelles techniques analytiques.
- « AlphaFold » et prix Nobel 2024 : confirmation de la révolution que représente l’IA dans la prédiction des structures protéiques.
- Cas Navalny : l’épibatidine, molécule analgésique extraite d’une grenouille équatorienne, aurait été utilisée sous forme synthétique comme poison. Illustration de la double nature (remède/poison) des substances naturelles.
- Darwin et Lamarck : mise en perspective du modèle évolutif — l’arbre darwinien doit être relu à la lumière de la génomique moderne (transferts horizontaux de gènes), sans pour autant négliger l’apport fondamental de Lamarck, précurseur français de la théorie de l’évolution.
- Pour en savoir plus : séance dédiée aux « médicaments de la mer » à l’Académie nationale de Pharmacie en 2024 : voir ici !
Découvrez + de 1100 textes des conférences du CDI sur le site du CDI de Garches
Vos commentaires et vos conseils contribuent à l’amélioration de nos parutions.
Vous disposez de l’espace « COMMENTAIRES » ci-dessous pour les exprimer.
Merci et à bientôt pour votre prochaine visite.

Laisser un commentaire