
Thèmes : médecine.
Conférence du mardi 9 décembre 1986.
Actualité et avenir des prothèses internes
et notamment en chirurgie cardio-vasculaire
Le mardi 9 décembre, Monsieur Cachera, Chef de service de chirurgie thoracique et cardio-vasculaire de l’Hôpital Henri-Mondor, Professeur à l’Université Paris XII, Directeur et Fondateur du Centre de recherches chirurgicales de cette même université, a, pendant une heure et demie, passionné l’auditoire venu nombreux l’écouter.
HISTORIQUE.
La chirurgie cardio-vasculaire actuelle est née grâce à la circulation extra-corporelle, c’est-à-dire la machine cœur-poumon. Cette machine est un vieux rêve du corps médical pour qui assécher les cavités cardiaques, intervenir sur le cœur, était quelque chose de presque mythique.
De nombreux chirurgiens y ont rêvé dans le passé, mais les techniques de l’époque ne permettaient pas l’ébauche même d’un projet.
Cependant, entre les 2 guerres mondiales, un homme mérite que l’on cite son nom car ce fut une sorte de visionnaire, de précurseur de toute la chirurgie cardiaque d’aujourd’hui. C’est Alexis Carrel qui remporta le prix Nobel pour ses travaux aux U.S.A. Il imagina vers les années 1920 que l’on pourrait un jour construire une machine qui permettrait de dériver la circulation sanguine, de court-circuiter le cœur et ainsi, de pouvoir aborder les cavités cardiaques pour y faire des interventions réparatrices.
Il s’était associé à Charles Lindbergh.
Ils construisirent une machine dont le moteur fut construit par Lindbergh et toute la tuyauterie conçue par Carrel.
Ils essayèrent cet appareil sur des chiens. Leur désillusion fut grande car ils virent qu’au bout de quelques minutes de fonctionnement de cet appareil, dans les tubulures de verre et de caoutchouc, le sang se mettait très rapidement à prendre en gelée et obstruait les cavités de l’appareil. Il leur manquait en effet une clé fondamentale.
En 1942, des chercheurs américains ont découvert l’héparine. Cette substance secrétée par le foie empêche le sang de coaguler.
John Gibbon, après la découverte de l’héparine, travailla pour mettre au point une machine qui était composée d’une pompe et d’un poumon artificiel. En 1955, il réalisa la 1ère circulation extra-corporelle chez l’homme.
Dès ce moment-là, un pas immense était franchi. La machine de Gibbon fut très rapidement utilisée par d’autres chirurgiens cardio-vasculaires, notamment ceux de la Mayo-clinique aux U.S.A. qui développèrent cette technique et aboutirent en moins de 2 ans à un lot très important de jeunes malades opérés (maladie bleue). Dès lors, dans le monde entier, des centres de chirurgie cardio-vasculaire s’ouvrirent, en France autour de Ch. Dubost …
Il est amusant de constater que les progrès d’équipement en matière de chirurgie cardio-vasculaire ont subi à peu près la même évolution que les équipements en matière civile.
SYSTÈME CŒUR-POUMON.
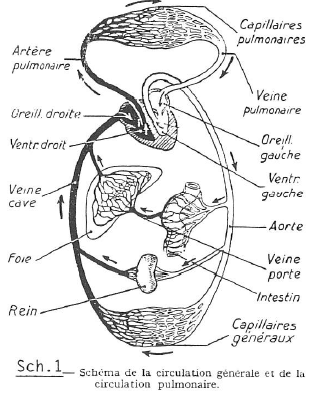
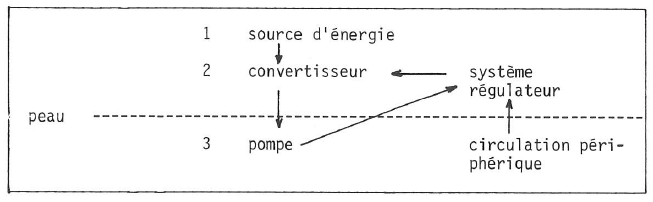
Pour comprendre ce qu’est la circulation extra-corporelle, il faut réaliser que l’objectif est de remplacer l’ensemble complexe formé par le cœur et le poumon. Il s’agit de deux ventricules reliés au poumon par les artères pulmonaires, le cœur étant la pompe véhiculant le sang à travers les vaisseaux et le poumon, le système d’oxygénation qui permet de saturer à nouveau en oxygène le sang qui parvient de la périphérie. Il arrive noirâtre, bleu dans les poumons et en ressort rouge vif. Le cœur fournit l’énergie motrice (schéma 1).
Tout système de remplacement cœur-poumon obéit au schéma suivant. Des tubulures recueillent le sang veineux dans les cavités cardiaques et le drainent vers un système d’oxygénation artificielle. Dans ce système d’oxygénation artificielle, le sang passe de la couleur bleue à la couleur rouge.
Il sera pris à la sortie par une pompe à rotor qui pousse le sang vers la tubulure de sortie.
Il est réinjecté dans le système artériel du sujet (schéma 2).
Les systèmes d’oxygénation par lesquels les chirurgiens ont commencé à travailler sont dits à « bulleur ». Ils comprennent une colonne dans laquelle arrive une tubulure d’oxygène. Par simple barbotage dans la colonne, le sang veineux forme une sorte de mousse qui peu à peu va réaliser le mélange d’oxygène, la saturation en oxygène étant réalisée à l’extrémité supérieure de la colonne où se trouve un système de débullage. A la sortie du système d’oxygénation, une pompe à galets pousse le sang à l’intérieur des tubulures. Un échangeur thermique ensuite permet de réchauffer ou d’abaisser la température du sang artériel à volonté. A l’heure actuelle la plupart des circulations extra-corporelles se font en hypothermie plus ou moins profonde. La température du sujet est abaissée aux environs de 20 à 25°.
Des progrès très rapides sont intervenus. Le premier fut de construire des oxygénateurs à usage unique et stériles. L’industrie biotechnologique s’est tout de suite intéressée à ce problème et a construit très rapidement des systèmes d’oxygénation qui ne servent qu’une fois et qui sont livrés stériles.
L’oxygénateur n’est plus ce réservoir de sang où barbotait l’oxygène, mais un dispositif où les échanges gazeux sont soigneusement contrôlés.
Il reproduit assez fidèlement l’alvéole pulmonaire naturelle. Une membrane, perméable aux gaz, sépare le sang d’un mélange gazeux riche en oxygène. Les transferts de l’oxygène et du gaz carbonique sont ajustables avec précision, en fonction des besoins du patient. L’interposition de la membrane entre le sang et le gaz évite tout contact direct, contact reconnu responsable de la dénaturation du sang dans les anciens oxygénateurs. Cette nouvelle génération d’équipements a permis d’allonger considérablement la durée de la période d’oxygénation et la circulation extra-corporelle autorisant ainsi une chirurgie moins précipitée.
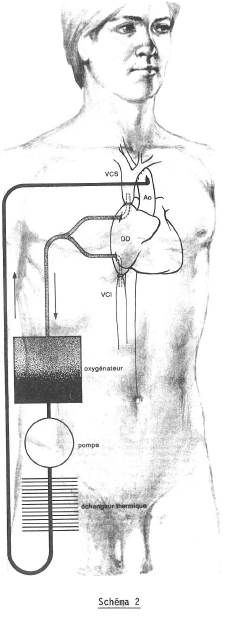
Schéma 2
On voit poindre maintenant des oxygénateurs de 3ème génération à fibres capillaires. Ce sont des microfilaments creux, construits dans le mème matériau que les membranes, mais au lieu que ce soit des membranes plates, pliées en accordéon, c’est une sorte d’écheveau de tout petits filaments. Le sang passe à l’extérieur de ces filaments et le gaz à l’intérieur de ces micro-tuyaux ; ainsi l’échange gazeux se fait exactement de la même façon qu’à travers une membrane mais avec une surface d’échange considérablement augmentée pour un volume considérablement réduit.
PROTHÈSES VASCULAIRES.
Les valves sont indispensables au bon fonctionnement cardiaque. C’est en effet par elles que les différentes cavités du cœur communiquent et que s’effectue le passage du sang. Leur fonctionnement peut être comparé à un clapet. Lorsque le sang s’accumule dans une cavité (oreillette ou ventricule), la pression s’élève et les valves s’ouvrent, permettant l’éjection du sang. En aval, la pression augmente et entraîne la fermeture de la valve. A la suite de processus infectieux ou dégénératifs, la structure des valves peut être altérée : déchirure, dépôt de calcaire, cicatrice fibreuse sont alors responsables d’une anomalie dans le jeu valvulaire.
L’ouverture peut être incomplète ou la fermeture incontinente. Dans tous les cas, la mécanique ventriculaire est altérée et l’évolution se fait plus ou moins vite, mais inéluctablement, vers l’insuffisance cardiaque.
Il faut changer dans ces cas-là la valvule.
Cela fait presque 30 ans que les chercheurs essaient de mettre au point des systèmes pour remplacer les valvules du cœur. Ils ont fait toutes sortes d’essais, avec du tissu, du caoutchouc, des silicones, en essayant d’imiter la nature en construisant des valvules le plus près possible de l’anatomie normale. Tout cela a donné beaucoup de déboires.
Un jeune chirurgien américain Albert Starr conçut une valve très simple qui faisait appel non pas à des clapets mais à une petite bille retenue par une cage. En 1961, il opéra 2 patients. Les opérations eurent un succès complet. Tout de suite cette valve a connu un succès légitime. Rapidement, elle fut utilisée dans le monde entier (fig. 3).
Ce n’est pas facile de construire une prothèse valvulaire. On est limité en premier lieu par la question des matériaux. Les valves humaines sont faites d’un tissu qui a une propriété de solidité extraordinaire.
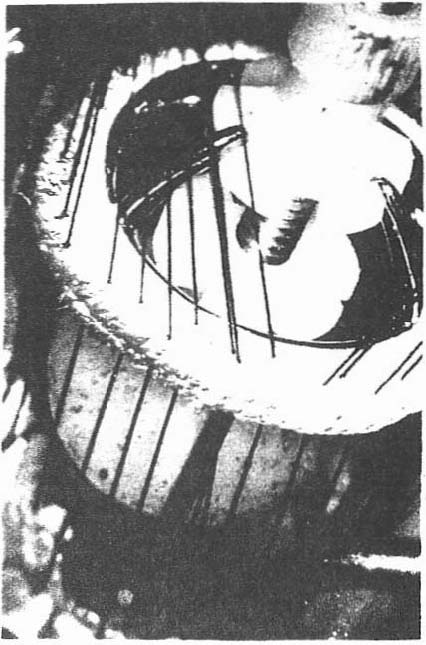
Figure 3
MATÉRIAUX UTILISES POUR LE REMPLACEMENT VALVULAIRE
I. – Substances synthétiques :
- alliages (titane)
- plastiques (téflon)
- silicones
- carbone
- graphite
II. – Tissus biologiques :
- tissus isogéniques (prélevés sur le patient lui-même)
- tissus allogéniques (prélevés dans l’espèce humaine)
- tissus xénogéniques (prélevés dans les autres espèces animales)
- porc,
- veau.
La valve de Starr a fait l’objet de recherches très approfondies.
Pour qu’une valve soit bonne, elle doit livrer passage au débit cardiaque (4 à 5 litres par minute au repos, jusqu’à 15 à 20 litres à l’effort). Il faut que le système d’occlusion soit très rapide, c’est-à-dire qu’il n’y ait pas de temps mort au moment de la fermeture pour que le sang n’ait pas le temps de refluer à travers la prothèse.
La prothèse a été au fil des années améliorée. Elle n’est pas parfaite et oblige les patients à se soumettre à un traitement anti-coagulant continu. Sans l’héparine, il n’y aurait pas de prothèse car le sang coagulerait autour du corps étranger que représente la valvule.
Pour répondre à cela, on a cherché à recouvrir les prothèses entièrement de tissus et à remplacer la bille par une bille métallique. Mais cette prothèse s’est avérée moins bonne chez l’homme.
On a ensuite imaginé les prothèses à disque basculant (figure 4). Elle a le défaut de faire du bruit.

Figure 4
L’inconvénient de ces prothèses mécaniques est le risque d’accident thrombo-embolique minimisé par la prise d’anticoagulant.
Des chercheurs ont essayé de recourir à des tissus animaux.
On s’est d’abord adressé au porc car les caractéristiques de l’aorte du porc sont voisines de celle humaine (figure 5). Ce ne sont pas des greffes mais des prothèses biosynthétiques.
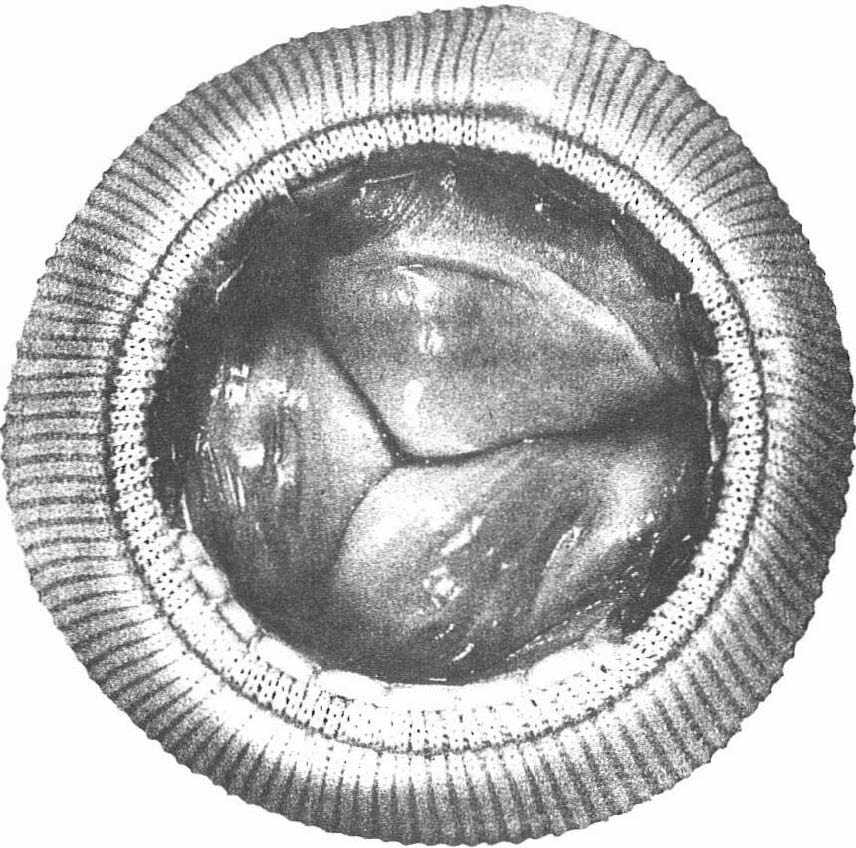
Figure 5
On ne peut pas laisser le tissu valvulaire du porc tel qu’il est. En effet, l’organisme est construit pour rejeter de façon très féroce toutes les particules qui proviennent d’une autre espèce et même d’un autre sujet humain. Notre immunité nous arme solidement contre toute intrusion d’une protéine étrangère. Si on laissait ces valvules en état, elles seraient très rapidement rejetées par le phénomène du rejet immunologique. Il faut donc tuer l’antigénicité de ces valvules par un traitement chimique. On fait une sorte de tannage. Celui-ci permettra la conservation durable de la souplesse des valves en les rendant neutres sur le plan immunologique. Les caractéristiques mécaniques de ces types de valves sont plus favorables que celles des prothèses car leur avantage essentiel est leur meilleure tolérance par le sang. Une réduction importante du risque d’accident thrombo-embolique, important avec les prothèses, a été observée avec ces bioprothèses. Elles seront donc utilisées plus volontiers chez les malades pour lesquels la poursuite définitive d’un traitement anti-coagulant est risquée.
L’inconvénient majeur de ces valves reste actuellement le risque d’altération de leur fonctionnement, par dépôts de calcaire.
SYSTÈMES OPTIQUES ET PONTAGES.
Les chirurgiens sont équipés de systèmes de grossissements optiques qui leur permettent de voir le champ opératoire multiplié par 5 et donc de réaliser des interventions microscopiques dont ils n’auraient pas été capables il y a quelques années.
Les artères coronaires ont un calibre de 2 à 3 mm et leurs branches collatérales de 1 à 1,5 mm. Ces techniques permettent de faire des pontages aorto-coronaires qui s’adressent à l’artériosclérose des artères coronaires (schéma 6).
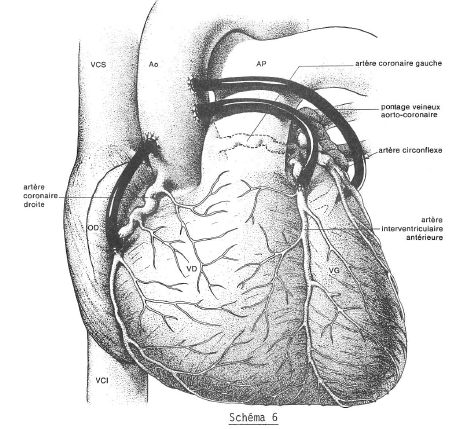
Ces pontages permettent de libérer le patient de toute douleur d’angine de poitrine et du risque d’infarctus. Pour le pontage coronaire, on se sert de petits morceaux veineux que l’on prélève chez le patient lui-même, à l’aide de ces segments de veine, on reconstruit une sorte d’artère artificielle entre l’aorte d’un côté et l’artère coronaire immédiatement en aval du segment occlus, de l’autre. Ce qui est difficile est de réaliser la couture qui a 6 à 7 mm de long et qui est faite avec des fils à la limite de la visibilité.
TRANSPLANTATION CARDIAQUE.
L’échec vérifié de toutes les techniques chirurgicales classiques ou l’impossibilité de leur réalisation en raison d’une déchéance cardiaque d’emblée excessive, impose au chirurgien un aveu d’impuissance et conduit à évoquer les possibilités du remplacement cardiaque total voire du remplacement cardio-pulmonaire complet si des lésions pulmonaires majeures sont associées au problème cardiaque.
La technique de la transplantation cardiaque a été préparée par une très longue approche expérimentale. L’une des difficultés est de préserver le système autonome du cœur. Il est dirigé par une espèce de petit ordinateur. Il y a 2 centres nerveux, le nœud de Tawara et le nœud sinusal (ou de Keith et Flack). Du nœud sinusal part un influx qui se propage dans la paroi de l’oreillette et donne l’impulsion au rythme cardiaque. Ce nœud de commande est sous l’influence du système nerveux ce qui explique que l’accélération puisse se faire à l’effort, au moment d’émotions, etc.
Le prélèvement du greffon cardiaque est réalisé actuellement selon la loi française chez tout sujet décédé qui répond aux normes médicales à condition qu’il ne soit pas porteur d’un document disant qu’il ne souhaite pas être donneur d’organes.
Nous sommes tous des donneurs d’organes potentiels.
La mise en place du cœur greffé est parfaitement réglée (schéma 7). « Ce n’est pas une opération très difficile. Ce qui l’est, c’est l’organisation totale, l’organisation du traitement. La « couture » n’est pas de loin la plus difficile des opérations mais elle a ce côté véritablement magique », nous dit le professeur Cachera.
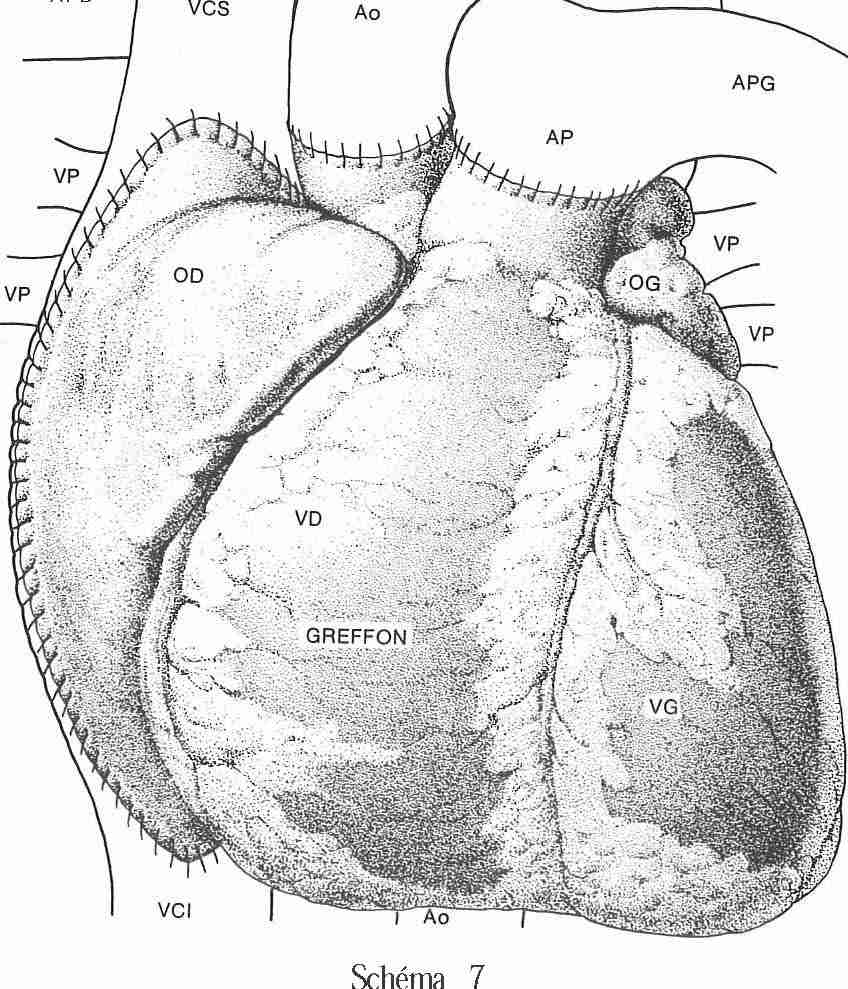
La transplantation cardiaque est devenue routine.
On estime à 300 le nombre de malades ayant subi une transplantation cardiaque. Ils retrouvent une vie socio-professionnelle quasi normale.
Les médecins disposent d’un nouveau médicament anti-rejet : la cyclosporine qui a été préparée à partir d’un champignon et qui limite les risques de rejet immunologique après greffe d’organe quel qu’il soit.
Nous avons reçu de nos ancêtres un patrimoine génétique codé qui fait qu’aucun être humain n’a tout à fait son semblable sur la planète excepté dans le cas d’un jumeau vrai homozygote (né de la division d’un même œuf).
Ceci explique que l’on met en jeu, lorsqu’on greffe un cœur, un double mécanisme de rejet :
- humoral par le jeu antigène, anticorps,
- cellulaire centré dans nos lymphocytes (certaines catégories de globules blancs).
Une certaine fraction des lymphocytes appelés lymphocytes T vont dans le greffon, reconnaissent la protéine étrangère et mettent en place un code contre ces cellules.
Un système de reconnaissance est donc mis en place dès les premières minutes de la greffe et ne cessera plus, ce qui explique que la tolérance de la greffe par l’hôte est une sorte de combat permanent au cours duquel il faut tenir en respect le phénomène de rejet, qui restera latent car il repose sur les bases mêmes du code génétique de l’homme ou de l’animal.
Après la période d’euphorie des années 68-69, a succédé une grande désillusion : un grand nombre des greffés devaient, après une amélioration spectaculaire de leur état, mourir par défaillance cardiaque due au rejet. La découverte de la cyclosporine en 1976 a permis de recommencer les greffes.
Les progrès réalisés dans la détection, la prévention et le traitement du rejet a en 1981 conduit à réaliser les premières greffes du bloc cœur-poumon.
Mais ce sont encore des opérations d’exception.
CŒUR ARTIFICIEL.
C’est l’un des rêves techniques né en même temps que la transplantation cardiaque, car on s’est rendu compte de la difficulté de la collecte d’organe et du phénomène de rejet que l’on tient en respect mais qui doit être contrôlé la vie durant.
Dès que l’on s’est penché sur le cahier des charges du cœur mécanique, on a été horrifié car cette pompe cardiaque qu’est le cœur est une merveille technique qu’il est très difficile de copier.
EXTRAIT DES CONTRAINTES :
1. Débit : rapidement variable de 5 à 15 l /min.
2. Pressions en amont < 10 mm Hg
3. Pressions : en aval entre 30 et 100 mm Hg
4. Volume total du sang : 0,5 à 1 l dans le thorax, 1 à 2 l dans l’abdomen
5. Densité : 1 à 1,5
6. Dégagement de chaleur < 40°
7. Matériau : hémocompatible
8. Durabilité : 40 millions de pulsations par an, 3000 millions ou 3 billions pour une vie moyenne
Des prototypes ont vu le jour. On en est aux tout premiers balbutiements car un cœur artificiel se compose de trois parties principales :
Seul le système de pompe est implanté (schéma 8).
La console pèse environ 150 à 200 kg, la longueur du tuyau n’excède pas 2 m. C’est dire qu’un patient chez qui on place un cœur artificiel de ce genre n’a aucune autonomie. Ce peut être une situation acceptable pour quelques heures ou quelques jours mais pas pour des durées prolongées.
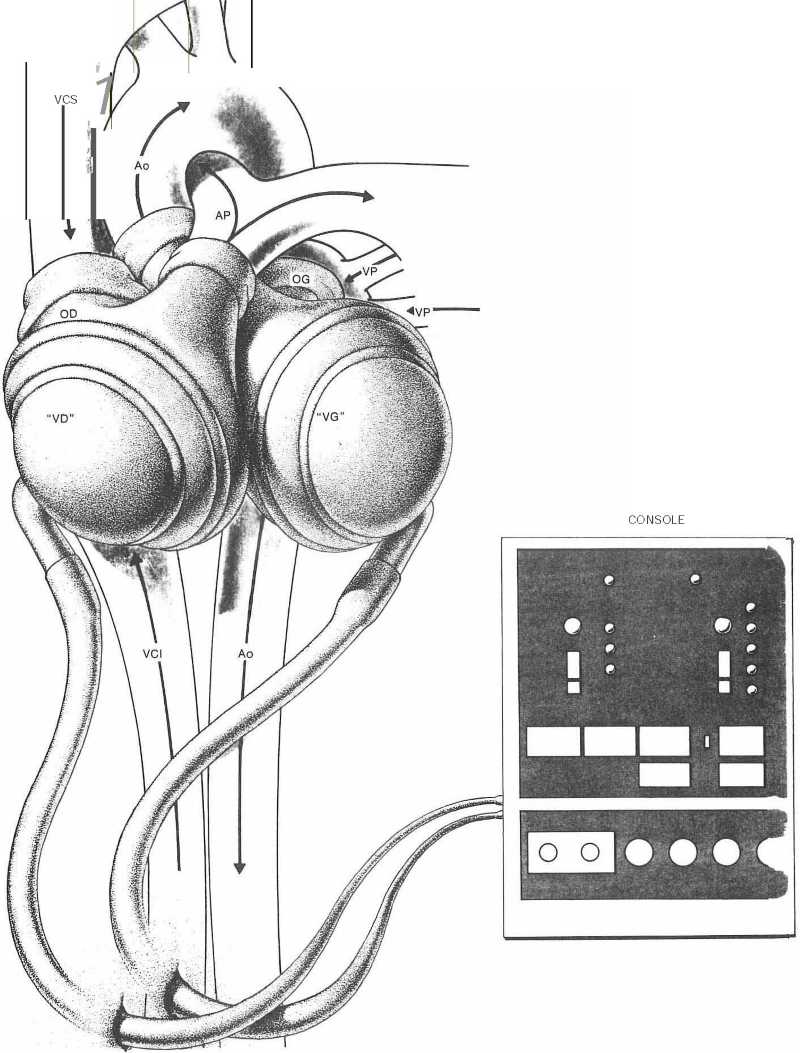
Schéma 8
On pense déjà au cœur artificiel de 2ème génération qui serait composé d’un système de pompe et d’activateur implanté. Seul le système transmetteur d’énergie serait extérieur avec par exemple des batteries qui pourraient être portées dans une ceinture.
PROBLÈMES SOCIO-ÉCONOMIQUES
1. Prix de revient :
- élevé (100 000 à 500 000 F.)
- difficile à prévoir
- maintenance
2. Étude de marché :
- difficile, 3000 cas par an (I.N.S.E.R.M.)
- fluctuant : arrivée imprévisible de nouveaux traitements
3. Prise en charge :
- sécurité sociale ?
- prix de journée ?
- contrats privés ?
En conclusion, on ne peut que méditer sur deux périodes :
- 1553-1628 : 75 ans pour passer de la découverte de la circulation pulmonaire (Servet) à celle de la circulation générale (Harvey).
- 1954-1967 : 13 ans de la 1ère intervention par « circulation extra-corporelle » à la 1ère transplantation du cœur de Barnard.
Découvrez + de 1100 textes des conférences du CDI sur le site du CDI de Garches
Vos commentaires et vos conseils contribuent à l’amélioration de nos parutions.
Vous disposez de l’espace « COMMENTAIRES » ci-dessous pour les exprimer.
Merci et à bientôt pour votre prochaine visite.

Laisser un commentaire