Thèmes : sciences.
Conférence du mardi 8 mars 1983.
Le 8 mars 1983, Monsieur de ROSNAY, directeur des applications de la recherche à l’Institut Pasteur, qui s’intéresse tout particulièrement aux technologies avancées, a prononcé une brillante conférence, devant une nombreuse assistance, sur « Les biotechnologies et notre avenir ».
Il a bien voulu rédiger lui-même le résumé de son exposé, ce dont nous le remercions vivement.
Je vous propose de diviser cette communication sur la bioindustrie en trois grands chapitres :
- Un premier chapitre consacré à l’historique de ces nouvelles technologies et à fournir les éléments de base pour comprendre les biotechnologies, la bioindustrie (comme toujours, dans les nouvelles disciplines, il y a des problèmes de vocabulaire et un certain nombre de principes de base peu familiers sur lesquels on doit s’étendre quelque peu) ;
- Le second chapitre sera consacré à des applications pratiques : qu’est-ce qui se fait dans tel domaine ? Quels sont les industriels déjà engagés dans les biotechnologies en France et à l’échelle internationale ? Quels sont les produits que l’on attend et ceux déjà proposés par ces industriels ?
- Enfin, le troisième chapitre sera consacré à la stratégie, aux efforts de la France par rapport aux autres pays, aux problèmes posés par la concurrence internationale, notamment vis-à-vis du Japon et des Etats-Unis ; aux moyens dont nous disposons pour être compétitifs ; aux avantages et aux difficultés que nous rencontrons dans ce domaine.
I. – L’ASPECT HISTORIQUE, ET EN MÊME TEMPS, DIDACTIQUE DES BIOTECHNOLOGIES.
On parle beaucoup de la biologie. Dans le grand public, au niveau des gouvernements, dans l’industrie, parce que c’est une discipline qui est en train, comme l’électronique, issue de la physique, de modifier les conditions de production dans certains grands processus industriels d’aujourd’hui : agriculture, chimie, santé notamment.
On en parle beaucoup, mais les biotechnologies existent depuis fort longtemps. On fabrique du pain grâce à des levures qui sont des micro-organismes. On fabrique de la bière, du vin ; on sait faire fermenter des aliments ; on sait même protéger les aliments contre la destruction microbienne grâce à des fermentations qui créent un milieu acide, empêchant d’autres bactéries de venir infester ce milieu ; c’est le cas du yaourt par exemple qui est un aliment fermenté, empêchant d’autres micro-organismes de venir l’utiliser comme milieu de culture.
Depuis des millénaires l’homme utilise donc les biotechnologies. Il les utilisait en fait sans le savoir. Il savait récolter des microbes pour les mettre au travail mais il ne connaissait pas les propriétés de ces microbes, ni comment ils étaient structurés, organisés, ni comment il pouvait les modifier.
Deux évènements à presqu’un siècle d’écart sont venus éclairer les mécanismes d’action des micro-organismes. Ce sont, bien entendu, les travaux de Pasteur d’une part et d’autre part, ceux de l’école de la biologie moléculaire représentée par Jacques MONOD.
D’abord Louis Pasteur parce qu’il a montré que des processus qu’on croyait chimiques à l’époque étaient en fait dûs à des micro-organismes : les « germes », les microbes, pas toujours pathogènes et le plus souvent utiles. Ces microbes, Pasteur les a identifiés, il en a démontré les modes d’action et les rôles multiples.
En fait, il a fait reculer les limites de la vie à l’échelle microscopique, préparant par là le pont ensuite créé par l’école de la biologie moléculaire, celle de Jacques MONOD près de 100 ans plus tard. Un pont entre le monde de la physique et celui de la biologie.
Pour employer une image, je dirais que les biologistes sont « descendus » dans les structures du vivant, du corps jusqu’à la cellule, entité minuscule à la base de toute vie.
Notre corps abrite près de 60.000 milliards de cellules sans compter tous les microbes qui y vivent, notamment dans notre côlon.
A partir de cette entité ultime qu’est la cellule, on pensait qu’on ne pouvait pas aller beaucoup plus loin à moins de faire la liaison avec les physiciens et les chimistes qui, eux, « remontaient » du monde des molécules vers la cellule.
C’est ainsi que s’est créée, dans les années 1950, une « tête de pont », pour parler comme les militaires, entre le monde de la physique, de la chimie et celui des biologistes.
Cette « tête de pont » s’est constituée au sein même de la cellule vivante ; c’est à ce niveau qu’on peut mieux comprendre les mécanismes de base qui conditionnent le fonctionnement cellulaire, la manière dont l’information est échangée entre les cellules, ou stockée ; la manière dont la cellule fabrique les substances dont elle a besoin et arrête cette fabrication lorsque la production a atteint un niveau satisfaisant.
Ces connaissances conduisent à ce que l’on appelle aujourd’hui, peut-être d’un terme un peu journalistique mais qui illustre bien notre propos, une véritable révolution biologique.
PASTEUR, d’une part et les micro-organismes, Jacques MONOD, d’autre part et l’interprétation de la vie en termes moléculaires.
Ceci nous conduit à la base de la révolution biologique qui, à mes yeux, est la suivante : nous avons peut-être compris dans les vingt dernières années que la révolution biologique est en fait une révolution dans la communication : comment les cellules communiquent-elles entre elles ? Quels sont les signaux qu’elles échangent ? Comment les molécules communiquent-elles entre elles à l’intérieur même des cellules ?
Révolution dans la communication mais aussi révolution dans la compréhension des codes qui sont à la base de cette communication. Les cellules utilisent en effet un langage codé.
Il y a un « langage moléculaire ». Les cellules échangent de l’information comme nous le faisons avec des mots, des lettres, des symboles, des signes, des images ; mais elles échangent des informations sous la forme de molécules codées qui transportent l’information dans leurs formes. En fait, la communication, au niveau biologique, est fruste et rudimentaire. L’information, c’est la forme. Une molécule possède une certaine forme, elle sera reconnue par une autre forme complémentaire.
De même qu’une clé est reconnue par une serrure dans laquelle elle produit une action : ouvrir la porte. Il y a complémentarité de la clé et de la serrure. L’information biologique est donc transmise sous une forme codée par la structure que les molécules prennent dans l’espace.
Un moyen de stocker de l’information, c’est une mémoire. Un moyen de reconnaître cette information, c’est un récepteur. Un moyen de véhiculer l’information, c’est un signal chimique (hormone ou médiateur).
Après avoir mieux compris la base de ces communications et de ces codes, les biologistes se sont posé la question suivante : pouvons-nous intervenir à l’échelle microscopique, à l’échelle moléculaire dans ces communications ?
Pouvons-nous modifier ces codes, envoyer des signaux à la cellule ; en fait, pouvons-nous à notre échelle communiquer avec elle ?
Est-il possible de la considérer comme une usine, une machine et lui donner des instructions pour lui faire fabriquer des substances qu’elle ne fabriquait pas normalement, dont la société a besoin et qu’il est extrêmement difficile de se procurer par les moyens classiques ?
C’est une question d’une importance capitale. Non seulement pour la recherche fondamentale mais aussi pour les applications industrielles.
Pour la première fois, l’homme serait capable d’envoyer à des êtres microscopiques qu’il ne voit même pas, les microbes et les cellules, des signaux tellement précis qu’ils pourraient être exécutés par ces micro-organismes, comme le ferait une machine.
C’est un défi extraordinaire que la biologie a réussi à traduire en expériences et en succès scientifiques. Aujourd’hui les biologistes communiquent avec les cellules, avec les microbes, et dans leur propre langage. Ils leur envoient des instructions, des programmes ; leur font exécuter des tâches que l’évolution ne leur avait pas appris à faire. Voilà la base de la révolution biologique. C’est ce que l’on appelle aujourd’hui le « génie génétique », ou les « recombinaisons génétiques ».
Il faut faire un pas de plus, essayer de comprendre comment les biologistes font exécuter ces programmes, comment ils transfèrent ces codes et pourquoi il existe une telle compétition à l’échelle internationale pour le contrôle de ces codes des codes secrets, comme dans le domaine militaire.
Le problème se pose de la manière suivante : tous les êtres vivants, qu’il s’agisse de plantes, de microbes, d’un vivant complexe, animal, papillon ou insecte, portent le même système de codage et de transfert de l’information. Ce système de codage contenu dans une très grande molécule qu’on appelle l’A.D.N. (voir ci-après le texte que nous avons consacré à l’A.D.N. (avec ses quatre lettres) et à la synthèse des protéines (avec leurs vingt acides aminés)). L’acide désoxyribonucléique, présent dans le noyau de toutes les cellules, est (pour employer une image) le « programme » au sens informatique du terme. C’est ce « programme » qui fait marcher les différentes machines biologiques, et fabriquer les substances dont elles ont besoin. En effet, à des programmes, il y a les agents d’exécution : les machines. Cette machinerie est faite de molécules qu’on appelle des protéines et surtout des protéines spéciales qu’on appelle des enzymes. Ces enzymes exécutent des tâches complexes comme des myriades de petits chimistes à l’intérieur des cellules.
Comment faire pour que le bon programme soit correctement transmis aux agents d’exécution de l’A.D.N. ? C’est très difficile : le langage de l’A.D.N. contient quatre lettres, le langage des protéines, vingt. Il faut donc trouver le moyen de traduire ce langage de quatre lettres chimiques en un langage de vingt autres lettres chimiques. C’est ce que les biologistes ont réussi à faire depuis 1973 : à peine dix ans.
On en est aujourd’hui à la routine, surtout depuis 1976/1977, puisque le génie génétique est devenu un processus industriel.
Comment faisons-nous ? Il faut d’abord obtenir le programme correspondant à la protéine qu’on veut faire fabriquer. Ce programme, on peut certes l’isoler à partir de la cellule appropriée. On peut aussi le synthétiser. Il existe aujourd’hui, en effet, des machines automatiques qui permettent, en frappant sur un clavier le code chimique correspondant, de fabriquer des programmes génétiques sous la forme d’une séquence d’A.D.N.
Ce programme est ensuite introduit dans une cellule, laquelle va se mettre à produire la substance recherchée. Tout le problème est de l’introduire et de le faire traduire sans erreurs.
C’est un peu comme si, encore une image, on donnait une bande perforée d’ordinateur à des personnes qui ne savent ni la lire ni l’écrire : il faudrait qu’ils soient capables de décoder ce langage fait de trous dans du papier !
C’est pourtant ce que les biologistes ont réussi à faire. Ils ont introduit de tels programmes dans des bactéries, êtres vivants très rudimentaires mais qui comprennent le programme et se mettent à exécuter les ordres qu’on leur donne.
Voici donc les biologistes dans la situation des informaticiens. Imaginez que nous ayons un ordinateur pour chaque tâche : pour envoyer une fusée, pour faire de la comptabilité, pour conduire les processus d’une usine … Ce ne serait pas très pratique. On sait qu’on dispose de quelques grandes catégories d’ordinateurs, on change leurs programmes. Avec les microbes nous étions dans la même situation au début de la microbiologie.
On a isolé le microbe qui « savait » faire du pain ; celui qui savait fabriquer le yaourt ; un autre encore capable d’extraire les minerais dans les mines du Chili : on mettait le microbe en présence de sulfure de cuivre, il fabriquait des sulfates et précipitait le cuivre.
Il y avait des milliers d’exemples. On a ainsi construit des bibliothèques de microbes, des microthèques dans lesquelles on les rangeait ; chacun avait sa spécialité. Aujourd’hui, avec les techniques de codage, de reprogrammation, de transfert des instructions à l’échelle microscopique, il est possible de n’utiliser que quelques microbes de base qu’on sait cultiver, comme les colibacilles, les pseudomonas, les bacillus, les levures. Quatre ou cinq catégories de microbes à l’intérieur desquels on change les programmes, comme en informatique.
Et voici un bacillus qui va se mettre à fabriquer de l’insuline humaine, un colibacille qui va fabriquer de l’interféron.
Voici encore une levure qui va se mettre à fabriquer un futur vaccin contre l’hépatite B humaine.
Reprogrammation mais aussi capacité, sans laquelle on ne comprend pas la biotechnologie, de reproduction de ces usines miniatures. N’oubliez pas qu’une bactérie c’est une usine. Elle assimile quelques éléments très simples et fabrique des molécules d’une complexité extraordinaire. Mais à la différence d’une usine, comme celles que nous connaissons, elle se reproduit. Lorsqu’on en fait une, on en fait des milliards. Pour vous faire une idée de la vitesse de reproduction des bactéries, sachez qu’elles doublent toutes les vingt minutes. Au bout de trois heures environ leur nombre s’est trouvé multiplié par 1.000. A partir d’un fermenteur de 100 mètres cubes, on peut produire en 24 heures des tonnes de bactéries.
Voilà donc une usine, une fois reprogrammée, qui va reproduire – j’insiste sur ce point important – non pas seulement à l’échelle de l’éprouvette ou du laboratoire, mais à l’échelle industrielle.
Nous sommes donc passés d’une bactérie qui ne mesure mème pas un micron à un fermenteur dont certains, au Japon notamment, ont des capacités de plusieurs centaines de mètres cubes. Ce qui permet de produire des tonnes de substances nouvelles une fois que les bactéries ont été correctement programmées.
Voilà donc les deux éléments sur lesquels je voulais insister au plan didactique : la possibilité de reprogrammation de la vie à partir d’une meilleure connaissance des langages moléculaires, et la possibilité de démultiplication de ces usines vivantes qui font passer aujourd’hui la biologie du stade du laboratoire à celui de la bioindustrie, dont nous allons maintenant parler.
Quels sont les grands secteurs d’application de cette bioindustrie ? Ils au nombre de cinq : il y a d’abord le domaine agro-alimentaire, je vais vous en donner des exemples ; ensuite le domaine de la santé (pharmacie, diagnostics…) ; en troisième lieu celui de la chimie, domaine important qui fait aujourd’hui appel à des matières premières coûteuses et pour lequel, grâce aux microbes, on utilisera bientôt des matières renouvelables.
Il y a ensuite le domaine de l’énergie. Un microbe est quelque chose d’infime, mais des milliards de microbes peuvent avoir un impact non négligeable sur la production énergétique, puisqu’ils sont à la base de la production de méthane, par exemple, ou d’alcool, lequel peut servir de carburant.
Enfin, cinquième secteur et non des moindres, celui de l’environnement, avec la possibilité de détruire des déchets émis par des industries, soit par des villes, grâce à des microbes spécialisés, capables de transformer des déchets toxiques en produits inoffensifs pour l’environnement.
Nous allons revenir successivement sur ces cinq secteurs.
D’abord le domaine de l’agro-alimentaire. Il n’y a pas assez de protéines pour nourrir les habitants du Tiers Monde. Pour obtenir plus de protéines ,il y a différents moyens : on peut accroître le rendement des récoltes grâce à des engrais appropriés ; on peut éviter que des prédateurs ne détruisent les récoltes grâce à des biopesticides adaptés. On peut également modifier génétiquement les plantes et leur donner des propriétés qui permettraient de les cultiver dans des terres arides.
Reprenons ces trois moyens : tout d’abord, produire des protéines. On a parlé, il y a quelques années du « bifteck de pétrole ».
De quoi s’agissait-il ? Il s’agissait de faire croître des micro-organismes, des levures, sur des hydrocarbures. Ces levures se nourrissaient d’hydrocarbures et fabriquaient des protéines. Ces protéines sont tout à fait similaires aux protéines de la viande et des végétaux que l’on mange couramment. La seule différence est que ces micro-organismes ont poussé sur du pétrole, d’où le terme de « bifteck de pétrole » avec sa consonance peu agréable pour le consommateur.
Néanmoins, le procédé existe et fonctionne. Il a donné lieu à une collaboration étroite entre ingénieurs du pétrole et biologistes. Plusieurs entreprises se sont lancées dans ce domaine il y a environ 10 ans.
Malheureusement, pour des raisons d’ordre économique, à savoir l’accroissement important du prix du pétrole et la diminution du prix du soja, ces procédés ont été temporairement abandonnés puis repris, notamment en Allemagne par HOECHST et en Angleterre par I.C.I. à partir de méthanol. Il s’agit cette fois de faire pousser les micro-organismes sur une substance qui n’est pas trop coûteuse.
Je voudrais vous donner un chiffre pour comparer la production de protéines par les moyens classiques végétaux et animaux et la production de protéines par les micro-organismes.
Pour faire faire 500 g de protéines grâce à un bœuf de 500 Kg, il faudra environ 24 heures. Avec 500 Kg de bactéries poussant sur un milieu approprié comme le méthanol, on peut produire dans le même temps, 5 à 10 tonnes de protéines ! Et ceci, sans problèmes de main-d’œuvre, d’engrais ou de conditions atmosphériques …
Il y a donc là une telle différence d’ordre de grandeur que de nombreux pays se penchent actuellement sur les possibilités de faire produire des protéines par les micro-organismes. Le problème est d’ailleurs moins technique que culturel et social : comment distribuer ces protéines, et dans quel contexte international ?
Deuxième moyen : lutter contre les prédateurs ; on a lutté jusqu’à présent contre les prédateurs avec du D.D.T. et du lindane, produits chlorés, très toxiques pour l’environnement. Grâce aux biotechnologies, on se préoccupe aujourd’hui de fabriquer des biopesticides, c’est-à-dire des toxines très spécifiques, fabriquées par des bactéries et qui permettent de détruire sélectivement certaines larves d’insectes. La bactospéine, par exemple, qui n’est pas dangereuse pour le monde vivant, les plantes et les autres animaux pas plus que nous-mêmes et qui détruit sélectivement certaines larves d’insectes. Cette toxine est fabriquée aujourd’hui par des bactéries telles que le Bacillus thuringiensis. Cette bactérie peut être reprogrammée par les techniques de génie génétique.
A l’Institut Pasteur nous nous en préoccupons. Nous avons établi des contrats avec des entreprises industrielles pour développer ces biopesticides à l’échelle internationale.
Enfin, dernier moyen, toujours dans la catégorie de l’agro-alimentaire, on peut modifier la génétique des plantes. Dans quel sens ? Je donnerai un exemple précis. Aujourd’hui, pour cultiver des plantes telles que les céréales – maïs ou blé – il nous faut des engrais azotés. Or, ceux-ci coûtent cher en énergie, en transport, ils interviennent pour 15 à 20% du prix d’une culture intensive.
Mais il existe des plantes qui n’ont pas besoin d’engrais. Ce sont les légumineuses, la luzerne, le soja, les lentilles, les pois. D’ailleurs les paysans le savaient parfaitement bien lorsqu’ils pratiquaient l’assolement triennal : une friche, de la luzerne, du blé.
Pourquoi ? Parce que la luzerne capte l’azote de l’air, enrichissant le sol en azote, transformé ensuite en dérivés nitrés puis en acides aminés qui servent à fabriquer les protéines dont nous nous nourrissons. D’où l’idée des biologistes : ne pourrait-on pas utiliser ce même procédé et enrichir directement la plante en azote sans passer par les engrais azotés ? Peut-on lui donner la capacité de fixer l’azote de l’air (N2) et de le transformer en ammoniac (NH3) qui entre dans la composition des acides aminés ?
D’où une course, presque une guerre économique et scientifique à l’échelle internationale, pour réussir à introduire dans des graminées, mais, blé, etc. les gènes de fixation de l’azote nécessaire à la fabrication de l’enzyme nitrogénase, seule capable chez les micro-organismes qui vivent en symbiose avec les racines des légumineuses, de transformer l’azote de l’air en ammoniac.
A l’institut Pasteur nous étudions de tels micro-organismes. Nous avons isolé les gènes de microbes qui vivent dans les racines des plantes et nous essayons actuellement d’introduire ces gènes dans des cellules plus développées telles que des levures pour voir si elles sont capables de fixer l’azote.
On peut se rendre compte aisément de l’enjeu stratégique. Une plante comme une graminée capable de pousser sans engrais, c’est déjà une promesse d’aliments à plus bas prix. Mais imaginez qu’on fasse pousser de l’hévéa fixateur d’azote ; on disposerait ainsi d’une source d’hydrocarbures et plus seulement d’aliments.
La biotechnologie peut donc conduire à modifier les rendements protéiniques agricoles dans des délais assez brefs. Ces expériences sont réalisées aujourd’hui par des entreprises industrielles créées pour exploiter ces techniques, en particulier « AGRIGENETICS » aux États-Unis qui cherche à développer ce type de technologie.
La deuxième catégorie d’application est la santé, la biopharmacie. Vous connaissez certains exemples pour les avoir lus dans la grande presse. On a parlé récemment, en effet, de l’interféron fabriqué par des bactéries ; de l’insuline humaine fabriquée par le colibacille et qui va être commercialisée au début de l’année prochaine pour les diabétiques ; on a parlé également du vaccin contre l’hépatite B (il est très difficile d’extraire l’antigène qui sert à produire ce vaccin car il faut l’extraire du sérum de malades, alors qu’avec les techniques du génie génétique, on peut faire produire cet antigène par des cellules et non plus par des bactéries).
Nous avons franchi une étape importante à l’Institut Pasteur en réussissant à reprogrammer non seulement des bactéries mais des cellules eucaryotes (à noyau). Ces cellules ont évidemment des systèmes de lecture plus développés que la bactérie qui n’a pas de noyau. Elles fabriquent l’antigène adapté, prêt à faire un vaccin.
En médecine, en pharmacie, on a l’espoir de fabriquer par les recombinaisons génétiques des substances très difficiles à extraire. La biotechnologie conduit également à des appareillages, à des techniques de mesure, de contrôle, d’analyse qui sont en train de bouleverser les diagnostics hospitaliers, grâce à l’automatisation de méthodologies qui utilisent les principes même de la vie, c’est-à-dire la spécificité de reconnaissance des molécules entre elles.
Vous avez entendu parler des anticorps. Ce sont des substances fabriquées par notre organisme lorsqu’il est attaqué par une substance étrangère, un virus par exemple. Or les biologistes ont réussi à « dompter » ces anticorps, à les domestiquer, à leur attacher des produits toxiques capables d’aller détruire sélectivement une cellule devenue malade, sans toucher à celles qui se trouvent autour.
Ces anticorps peuvent être également utilisés pour analyser des substances présentes à l’état de traces infimes dans l’organisme.
La spécificité de la reconnaissance entre les anticorps et ces substances (les antigènes) est telle que si l’on attache à l’anticorps une « étiquette » radioactive ou une étiquette permettant de réaliser une réaction colorée (donc automatisable), cet anticorps « marqué » va aller dans l’organisme – comme la tête chercheuse d’une fusée Exocet miniature – chercher les molécules que l’on veut analyser, même s’il n’en existe que quelques-unes !
Imaginez que ces molécules soient le signe qu’un processus de cancérisation a commencé. On dispose ainsi, pour la première fois, de moyens permettant d’aller traquer dans l’organisme des substances signalant un cancer, de les localiser et de marquer l’endroit où débute la tumeur, avant qu’elle ne se manifeste à l’état où il faudrait normalement l’opérer.
Voilà donc un exemple, en biopharmacie, des applications des biotechnologies : ces anticorps « têtes chercheuses » appelés anticorps monoclonaux.
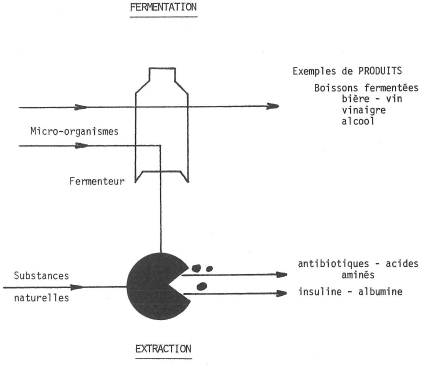
Troisième catégorie, celle de l’énergie. Le méthane, gaz combustible, est fabriqué par des micro-organismes. En faisant fermenter des déchets agro-alimentaires, on obtient en effet du gaz méthane, capable de faire fonctionner des moteurs. Les rendements jusqu’à présent sont peu satisfaisants et les conditions d’utilisation peu agréables. Même s’il existe 7 millions et demi de « digesteurs » à méthane en Chine, nous ne sommes pas prêts de transposer en Europe les procédés dans la campagne chinoise !
Ces biotechnologies permettent de perfectionner les processus et d’améliorer les rendements. Des digesteurs plus simples, plus faciles à utiliser pour des fermes, des habitations, ont été développés.
L’alcool est fabriqué par des levures qui nous donnent le champagne, ou le vin de Bourgogne. Mais cet alcool n’est pas utilisable directement dans des moteurs. Il faut un alcool pur déshydraté. Cet alcool est aussi performant que l’essence, même si on le mélange parfois à celle-ci.
Les levures sont donc les éléments déterminants de la production d’alcool. Malheureusement ; elles ont un défaut, elles ne « savent » pas transformer la cellulose, les déchets lignocellulosiques de l‘agriculture en alcool. Elles n’ont pas les enzymes nécessaires pour agir directement sur la cellulose. Pour faire de l’alcool, elles ne savent travailler qu’à partir des sucres, en réalisant la fermentation des jus sucrés. Par contre, on connaît des bactéries qui transforment la cellulose, la digèrent, la dégradent en petites molécules, et par fermentation transforment ces petites molécules en alcool.
Le rendement d’une bactérie à côté de celui d’une levure est faible : une levure parvient à fabriquer jusqu’à d’alcool dans le milieu où elle se trouve, alors que la bactérie n’en fabrique que 4 à 5%. De plus, la bactérie est inhibée par sa propre production d’alcool.
D’où l’idée, expérimentée dans plusieurs laboratoires, de transférer dans la levure les gènes de bactérie permettant de fabriquer les enzymes qui dégradent la cellulose. On disposerait ainsi d’une levure capable de transformer les déchets agricoles et de produire de l’alcool pouvant être utilisé comme carburant.
Voilà deux exemples dans le domaine énergétique. Je passerai plus rapidement sur les autres catégories, celles concernant l’environnement et la chimie.
L’environnement : les bactéries qui dégradent les substances toxiques existent déjà : un bassin de traitement biologique est un moyen d’utiliser les microbes pour transformer des produits organiques en eau, gaz carbonique, hydrogène ou méthane.
Aujourd’hui, en connaissant mieux les enzymes qui sont à la base de ces différents processus, on est capable de faire croître des bactéries sur des milieux très agressifs, telles les eaux usées de l’industrie chimique. On peut ainsi faire croître des bactéries sur des phénols, des produits chlorés.
Elles induisent peu à peu la synthèse d’enzymes capables de détruire les substances dangereuses. Tout d’abord les biologistes ont sélectionné des souches capables de détruire des déchets dangereux. Ensuite, ayant étudié ces souches, ils ont réussi à localiser les gènes codants pour les enzymes destructrices des produits chimiques toxiques. Aujourd’hui, ils tentent de fabriquer par génie génétique des souches bactériennes disposant d’une batterie d’enzymes de dégradation. Ces techniques ouvrent de grands espoirs pour le recyclage des déchets.
Dans les domaines classiques de la chimie, les moyens portent aujourd’hui sur les dérivés pétroliers. L’éthylène est la base de départ de nombreuses substances. Les dérivés du cracking du pétrole conduisent à la plupart des matières plastiques que nous connaissons. Mais avec l’accroissement des coûts et la difficulté d’obtention des matières premières de base, il devient rentable de faire fabriquer par des micro-organismes, dans des conditions de culture satisfaisantes, des substances de base pour la chimie fine, puis pour la chimie lourde. Ces matières de base sont ainsi produites non pas à partir de dérivés de pétrole, mais de dérivés renouvelables, tels que la cellulose ou la lignine.
Je voudrais tirer une conclusion de ce second chapitre sur les applications pratiques au niveau industriel : il est en train de se créer dans le monde une compétition entre les surfaces destinées à l’alimentation du bétail et des êtres humains et les surfaces qui sont ou seront destinées à la production des matières premières de base pour la chimie ou les carburants.
Les hydrocarbures que nous utilisons aujourd’hui sont le résultat du stockage dans le sol de végétaux pendant plusieurs millions d’années. Si l’on veut remplacer ces carburants fossiles par des carburants renouvelables, il va falloir transformer du temps en espace, c’est-à-dire en surfaces. La feuille est en effet un capteur solaire assez performant, mais qui demande beaucoup d’espace. Pour faire des carburants renouvelables ou des matières premières de base pour la chimie, on sera donc obligé de cultiver de grandes surfaces agricoles. Il va donc se créer une compétition entre l’agro-alimentaire et l’agro-énergétique comme le disent les Américains : entre « food » et « fuel ».
Je voudrais attirer votre attention sur ces problèmes qui dépassent les frontières, les techniques, pour se poser en termes de système, c’est-à-dire nécessitant l’intégration de ces différents paramètres entre eux.
Ceci nous conduit à la troisième partie de mon exposé la partie stratégique. A l’échelle internationale, comment la France se situe-t-elle par rapport aux autres pays, quels sont les grands défis qui s’ouvrent à nous dans ce domaine ?
Il faut dire d’abord que la France a saisi assez tôt, dans la compétition internationale, le défi biotechnologique.
Nous avons mal pris le tournant de la microélectronique mais cette fois-ci nous sommes partants dans la course aux biotechnologies. Certains industriels de la chimie, de la santé, de la pharmacie, ont été pris de court, considérant qu’il s’agissait des techniques de l’an 2000 … Mais cela a été salutaire. Aujourd’hui il existe un effort conjugué des Pouvoirs Publics et des grandes entreprises pour établir un réseau de communications, d’échanges, d’expériences et d’essais de diversification, afin de placer la France dans la compétition internationale. Nous ne sommes pas en train de « rater le tournant », mais nous risquons de prendre du retard si nous ne mettons pas en œuvre un certain nombre d’actions prioritaires.
Un certain nombre de rapports sur la biologie ont été proposés ; le rapport « Sciences de la vie et Société » et son annexe « Biotechnologies et Bioindustries » que j’ai eu l’honneur de rédiger ; le rapport de Monsieur PELISSOLO, « La Biotechnologie, demain ? ». Des structures nouvelles ont été créées, telle que la Mission des biotechnologies auprès du ministère de la recherche et de la technologie, pour laquelle un budget important a été voté et des experts nommés. Un dispositif important a été mis en place, tant pour les incitations industrielles que pour les nouveaux programmes de recherche au niveau universitaire et la formation des bioingénieurs. Ce dispositif s’appuie sur des pôles biotechnologiques tels que Compiègne, l’Institut Pasteur, Toulouse, l’I.N.A. (Institut National Agronomique).
Des expériences de diversification intéressantes sont aujourd’hui tentées dans des entreprises.
Il y a schématiquement trois groupes d’industriels intéressés par les biotechnologies en France. D’abord, l’industrie pharmaceutique et l’industrie biologique qui produisent les vaccins, les antibiotiques, les hormones, et qui sont évidemment, au premier chef, concernées par ces nouvelles techniques.
Une deuxième catégorie peut-être moins connue, est représentée par les pétroliers, dont certains se sont lancés dans la production de protéines à partir de micro-organismes croissant sur des alcanes. Ce savoir-faire a contribué à pousser certaines entreprises pétrolières à se diversifier en biotechnologie. On connait les efforts entrepris par ELF Aquitaine notamment avec la création d’ELF-Bio industrie.
La troisième catégorie est constituée par le secteur agro-alimentaire. Par tradition, ce secteur plus fermé sur lui-même a certaines difficultés à intégrer les progrès de la biologie à l’échelle internationale. Aujourd’hui la biotechnologie fait irruption dans ce secteur. C’est un de ceux qui croit le plus rapidement à l’étranger, notamment au Japon et aux États-Unis.
On rencontre en France un certain nombre de problèmes d’ordre stratégique qui risquent de nous retarder par rapport à la concurrence internationale. Il s’agit surtout des difficultés de transfert des résultats du fondamental à l’appliqué, et plus généralement des relations entre l’université et l’industrie.
La situation s’est sensiblement améliorée au cours de ces dernières années, surtout lorsqu’il existe une communauté d’intérêts entre universitaires et industriels. Quand un contrat a été signé, précisant les intérêts des parties, les redevances, les conditions de publication, les brevets, les relations université-industrie se déroulent dans de bonnes conditions. Nous en avons l’expérience à Pasteur depuis cinq ou six ans. Il reste cependant un fossé un niveau du pré-développement.
Il y existe à ce stade un « no man’s land », un terrain qui n’appartient plus tout à fait à l’université, pas encore à l’industrie, et dans lequel beaucoup de projets tombent et se perdent.
Ce problème du pré-développement est crucial dans notre pays, particulièrement pour la biotechnologie ; surtout parce que les biotechnologies ne sont pas une discipline. On définit en effet la biotechnologie comme la mise en œuvre des micro-organismes et des cellules pour la production de substances utiles à la société, la dégradation ou les transformations de déchets. Il s’agit donc de mise en œuvre de processus, grâce à une panoplie de moyens qui vont du génie génétique, aux cultures cellulaires, en passant par l’appareillage de contrôle, de synthèse ou d’analyse.
La biotechnologie ne constitue donc pas des secteurs bien définis à l’intérieur desquels on pourrait créer des structures de pré-développement comme dans l’industrie chimique, mais des interfaces diffus dans lesquels, d’une part, les disciplines ne sont pas clairement définies, d’autre part, le langage entre les industriels et les scientifiques n’est pas toujours adapté.
Qu’est-il fait en France et à l’étranger pour essayer de surmonter le grave inconvénient du pré-développement en biotechnologie ?
En France, le Gouvernement a procédé à la création de « centres de transfert ». En relation avec l’I.N.S.E.R.M., l’I.N.R.A., le C.N.R.S. et l’Institut Pasteur a été créé un groupement d’intérêt économique, le G3 (Groupement Génie Génétique) qui a pour but d’effectuer des transferts à partir des souches bactériennes, fabriquées au laboratoire, jusqu’au stade de la production pilote. Il s’agit en fait d’« optimiser » la souche, de lui faire produire avec un meilleur rendement, dans des meilleures conditions de culture, avec un prix de revient plus bas, un milieu moins coûteux ; en d’autres termes, à partir de la souche de laboratoire, de rechercher les procédés les plus économiques, ce qui n’intéresse pas toujours un chercheur mais un bioingénieur.
Nous revenons ainsi au problème de la formation des bioingénieurs, capables de penser les problèmes à la fin des recherches et au début de l’industrialisation ; capables de dialoguer avec les chercheurs, d’avoir présents à l’esprit les problèmes d’ordre économique, de rendement et de changement d’échelle.
La France part en ce domaine avec du retard. Autant nous sommes partis juste à temps dans la course des biotechnologies, autant nous prenons du retard pour la formation des hommes. Nous avons des grandes écoles d’ingénieurs axées sur les mathématiques, la physique, l’ingénierie. Mais nous n’avons pas formé suffisamment d’hommes aux sciences de la vie. Probablement parce que les sciences de la vie ont été considérées comme une discipline mineure après les sciences physiques et chimiques considérées comme plus nobles, car plus abstraites. La biologie se trouvait cantonnée à l’assistance pour la médecine : les « biologistes » du laboratoire d’analyse, et non considérée comme un pouvoir nouveau en train de naître, capable de modifier l’industrie et nécessitant par conséquent la formation d’hommes adaptés à ces nouveaux défis. C’est pourquoi nous constatons un retard qui sera peut-être difficile à rattraper.
La France forme actuellement 200 à 300 bioingénieurs et techniciens par an, tandis que le Japon en forme 6.000 et les États-Unis 30.000.
Que font les autres pays pour améliorer les transferts entre le fondamental et l’appliqué et combler ainsi le fossé qui existe entre l’université et l’industrie ?
Ils ont recours à des systèmes d’échange plus flexibles que les nôtres. Il s’agit plus, en France, d’un problème de structures que d’un problème de financement. Au Japon, les associations d’anciens élèves de l’université travaillant dans l’industrie sont très puissantes. Il n’y a pas de frontières réelles entre l’université et les chercheurs industriels. Il y a des échanges constants entre les uns et les autres.
Aux États-Unis, les chercheurs universitaires passent des contrats avec l’industrie, puis fondent parfois leur propre entreprise dont ils restent consultants ou même parfois actionnaires. A l’heure actuelle se posent toutefois des problèmes notamment sur le plan éthique : un chercheur peut-il continuer à travailler dans un laboratoire financé sur fonds publics, alors qu’il est actionnaire de sa propre entreprise de génie génétique ? Néanmoins, cette interface féconde entre l’industrie et l’université, le foisonnement d’entreprises nouvelles aux États-Unis, les associations professionnelles d’anciens élèves au Japon, créent un climat qui accélère le développement des biotechnologies.
Les contrats, les transferts, les retombées industrielles sont irrigués par la source des informations et des innovations venant, en grande partie, de l’université.
Nous avons donc à faire face à un défi au plan technologique et maintenant au plan industriel. En effet, des produits nouveaux arrivent sur le marché : exemple, des sucres alimentaires obtenus aujourd’hui à partir du fructose grâce à des enzymes fixés sur des colonnes. La place sur le marché de ces sucres s’accroît rapidement et déplace stratégiquement celle du sucre traditionnel de betterave ou de canne.
Comment la France fait-elle face à cette compétition ?
Je pense que nous risquons de nous engager dans une voie qui me parait dangereuse : nous continuons à penser les biotechnologies en termes de disciplines, et par conséquent en termes de « créneaux ». Cela fait partie de notre approche cartésienne : nous pensons en termes de territoires et de secteurs plutôt qu’en termes de filières. Une approche en secteur consiste à privilégier prioritairement telle discipline et, à l’intérieur de celle-ci, à choisir des « créneaux ». On fait ainsi porter les priorités financières ou humaines sur tel facteur au détriment d’autres. On isole du système dans lequel se trouve le secteur considéré, un élément ponctuel sur lequel on va faire porter tout le poids de la décision.
Une approche en « filière » est tout à fait différente. Elle consiste à rechercher la logistique et les moyens techniques indispensables à différents domaines et de jouer sur plusieurs facteurs à la fois, de manière à renforcer les filières et la logistique, les unes par les autres. Je reprendrai un exemple militaire : il y a la stratégie, la tactique et la logistique. On ne peut pas privilégier l’une par rapport à l’autre. Si l’on n’a pas la logistique, on échoue à terme. En adoptant une optique purement sectorielle, on risque de négliger la tactique. On fait des actions spectaculaires, mais on risque de perdre à terme.
Par contre en réalisant des actions peut-être moins spectaculaires, telles que de faire renaître en France une véritable industrie des fermentations, de relancer l’instrumentation d’analyse, de contrôle chimiques, ou de développer les communications des bulletins de liaison, les colloques, les congrès, on favorise les moyens logistiques et l’échange d’informations, les communications sans lesquels il n’y a pas d’innovations.
C’est ce qu’ont apparemment compris nos concurrents à l’échelle internationale : la communication est facteur d’innovation. Il semble que dans notre pays nous ayons tendance à nous isoler. Et ceci en raison de différents facteurs : la langue, les difficultés d’exportation, de communication avec l’étranger, qui au fond nous inhibent, nous empêchent d’être compétitifs dans des secteurs où nous sommes pourtant partis en même temps que les autres.
Voilà quelques exemples de barrières qui posent des problèmes à l’échelle nationale et internationale.
Je terminerai cet exposé sur une ouverture vers l’avenir. Vers quoi nous conduisent la biotechnologie et la bioindustrie naissantes ?
Je crois, toutes proportions gardées, que la révolution que nous vivons en ce XXème siècle a été due en partie aux découvertes de la physique. L’électricité, l’électronique, les transports ont bouleversé la société dans laquelle nous vivons. Ils résultent d’une « domestication » et du contrôle de l’énergie.
Nous entrons dans une ère où nous commençons à comprendre comment mieux domestiquer l’information. Ce que je vous ai dit sur les codes, les langages de.la vie doit s’appliquer à beaucoup d’autres domaines de notre société. Nous passons de l’agriculture et de la technoculture, à ce que j’appellerais l’« infoculture ». La biologie comme la microinformatique sont des sciences qui nécessitent une parfaite maîtrise de l’information. Ce que les Japonais ont peut-être compris avant les autres nations. Disposant, en effet, de faibles ressources naturelles, la maîtrise de l’information est considérée comme un moyen efficace pour créer des produits nouveaux et être compétitifs sur les marchés internationaux. Ce n’est pas un hasard si les Japonais ont fait, dans le domaine de la microinformatique de la biotechnologie, les grandes découvertes que l’on sait. Pour être compétitifs, innover, créer des emplois, développer nos industries de pointe, nous devons continuer à miser sur ces deux grands domaines de l’avenir : la biotechnologie et la microélectronique. Gardons également présent à l’esprit qu’il y a peut-être un mariage possible entre les deux. Se dessine en effet à l’horizon le rapprochement de l’informatique et de la biologie dans une série de domaines d’applications sur lesquels je ne pourrai m’étendre ici, et que j’ai appelés la « biotique ». Comme la bureautique ou la télématique, la biotique me paraît être à l’horizon 2000, un des grands secteurs de demain.
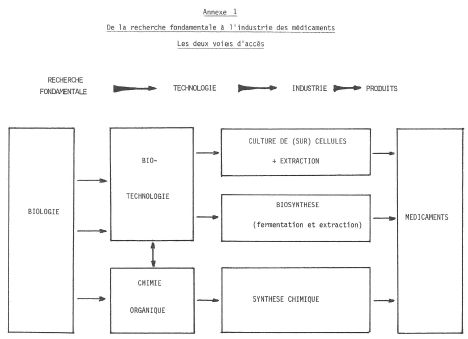
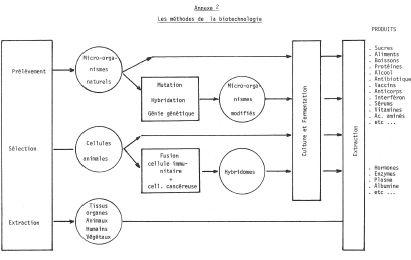
Annexe 3
Biologie industrielle
Deux opérations
ÉTUDE SOMMAIRE DE QUELQUES FACTEURS DE L’HEREDITE
par Marcel SIRE
Au cours de nombreuses conférences données au Cercle depuis mars 1979 sur la cellule, l’hérédité, les vaccins contre maladies virales, les biotechnologies, l’immunologie, l’origine et la nature de la vie, les greffes, les groupes sanguins, etc., les noms suivants ont été maintes fois prononcés :
- Chromosomes,
- Gènes,
- Acide désoxyribonucléique (ADN)
- Acides aminés,
- Protéides …
mais en ordre dispersé, sans vue d’ensemble ce qui a pu entraîner des imprécisions, sinon des confusions.
Dans les lignes qui suivent j’ai tenté une vue d’ensemble.
J’ai été amené à simplifier ; je pense que la plupart des adhérents suivront mon propos, en dehors des formules chimiques que j’ai mises à l’intention de ceux qui ont conservé un bon souvenir de la chimie. La lecture des passages soulignés d’un trait en marge est accessible à tous.
Nous serons brefs sur certaines questions alors que nous nous étendrons sur la molécule d’ADN.
LES CHROMOSOMES.
Les chromosomes sont des formations présentes dans le noyau de la cellule. Pratiquement invisibles dans la cellule au repos, les chromosomes deviennent colorables, donc visibles, dans la cellule en division.
Ils se présentent alors sous la forme de filaments. Dans la plupart des espèces, les cellules du corps ont deux jeux de chromosomes : 2n (23 paires chez l’Homme), (fig. 1). On les nomme diploïdes.
Au niveau moléculaire, l’analyse chimique établit que les chromosomes ont quatre constituants principaux :
- deux acides nucléiques :
- acide ribonucléique ARN, dont nous ne parlerons pas.
- acide désoxyribonucléique ADN, qui fera l’objet d’une étude particulière.
- deux groupes de protéines :
- des protéines liées aux ADN dans des molécules nucléoprotéiques,
- des protéines, qui n’existent pas sous cette forme, dont la quantité varie au cours de la vie de la cellule.
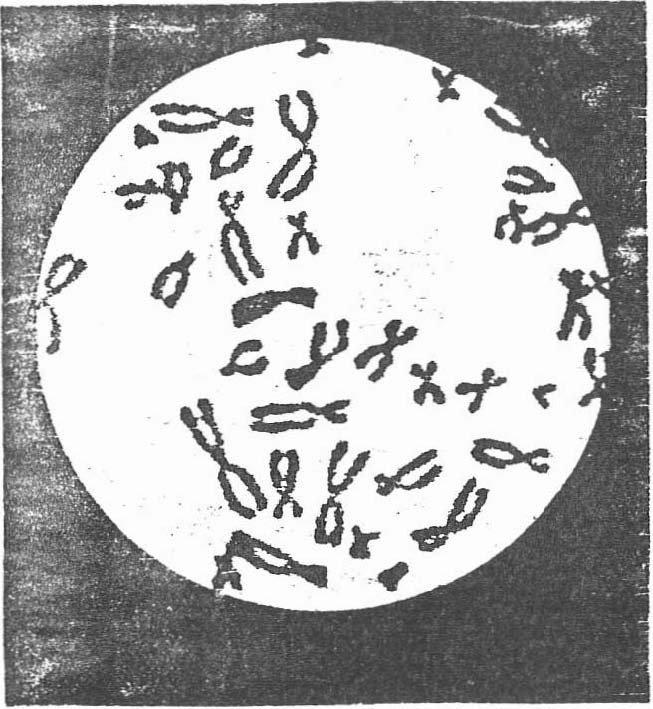
fig. 1. Chromosomes humains.
Microphotographie d’un noyau de cellule normale
LE GENE.
Le gène, traditionnellement, est une particule qui sert de support matériel au caractère héréditaire.
On sait aujourd’hui que le gène n’est autre qu’un segment de chromosome qui contrôle la synthèse d’une protéine active, protéine qui intervient dans la réalisation d’un caractère héréditaire. Le gène est donc l’unité mendélienne qui, transmise de générations en générations, assure la pérennité de l’information génétique, et donc du caractère héréditaire.
Le lieu où siège un gène sur un chromosome donné s’appelle locus ; toutes les mutations d’un même gène siègent toujours au même locus.
Chaque gène est donc un segment comprenant soit une molécule d’ADN, soit un nombre limité de celles-ci mises bout à bout.
Le gène est une unité de fonction qui est indissociable.
On peut donner l’équation :
Un gène = un caractère (par ex. la couleur des yeux).
L’ACIDE DÉSOXYRIBONUCLÉIQUE : ADN.
On pense maintenant que parmi les constituants du chromosome seul l’ADN représente le matériel génétique.
L’ADN est le support matériel de l’hérédité.
Nous verrons dans ce qui suit que l’ADN est :
- porteur d’informations figurées par l’ordre suivant lequel quatre types de bases AT, TA, GC, CG sont disposés tout au long de la double hélice qui forme la molécule d’ADN.
Nous verrons que ces informations sont en nombre considérable.
- capable de réplication : une séquence d’ADN est capable de se transmettre identique à elle-même au cours des divisions cellulaires successives.
La réplication est une véritable autocopie.
- apte à modifier sa structure par accidents lors de la réplication et donner naissance à des mutations qui sont des « erreurs de copie ».
LA STRUCTURE DE LA MOLÉCULE d’ADN.
1. Structure primaire.
a. – Deux limons LI et L2, parallèles, formés d’une suite de nucléotides (fig. 2).
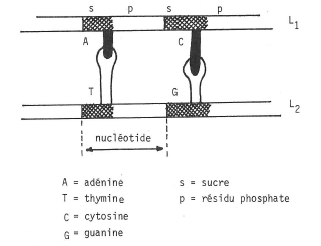
Fig.2. Schéma d’une portion d’ADN.
Chaque nucléotide comprend :
a) un sucre (s) à 5 atomes de carbone (le désoxyribose qui figure dans nos schémas sous le nom de ribose) ;
Le pentagone porte une fonction alcool primaire : CH2OH et une fonction alcool secondaire : CHOH
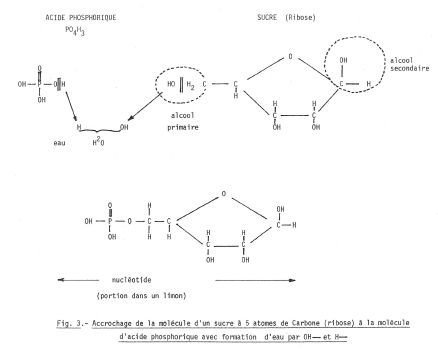
b) des restes d’acide phosphorique PO4H3 (p)
La fonction alcool secondaire CHOH permet la liaison avec les restes de l’acide phosphorique par combinaison d’un OH de la fonction alcool et d’un H de l’acide avec formation d’une molécule d’eau H2O.
Ainsi se forme un nucléotide avec un sucre un bout et le résidu phosphate l’autre (fig. 3).
b. – Les deux limons sont reliés par des barreaux d’égale longueur qui s’accrochent la hauteur de chaque sucre grâce la fonction alcool secondaire (CHOH) de celui-ci.
Chaque barreau est formé de 2 bases azotées qui appartiennent deux familles chimiques différentes (fig. 2) :
Bases puriques : adénine désigné par la lettre A, guanine par la lettre G
Bases pyridimiques : thymine désigné par la lettre T, cytosine par la lettre C
Les bases puriques sont plus courtes que les bases pyrimidiques ; les barreaux ont même longueur par accrochage l’une l’autre de bases des deux familles.
On a donc 4 types de barreaux :
AT
TA
GC
CG
L’ordre dans lequel les barreaux se suivent est variable :
AT GC CG AT CG GC TA AT … etc.
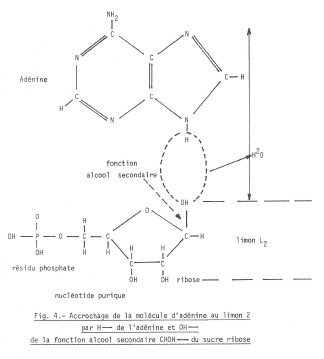
Le schéma (fig. 4) montre comment l’adénine s’accroche au limon 2 par la fonction alcool secondaire du sucre, avec formation d’une molécule d’eau H2O.
Le schéma (fig. 5) montre comment une base (ici l’adénine) s’accroche la base complémentaire (ici la thymine) par des liaisons hydrogène fragiles, facilement brisées.
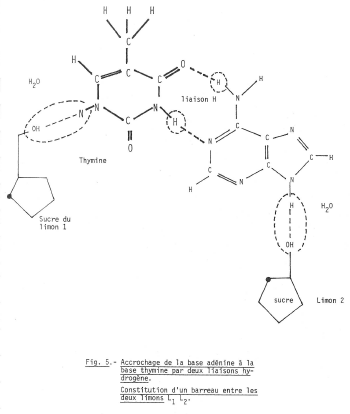
Lorsque les liaisons entre les bases AT et GC sont brisées, les deux limons L1 et L2 s’écartent (fig. 6) ; l’ouverture permet une copie ou la synthèse d’une nouvelle chaine possédant la même information = c’est la réplication que l’on observe au cours de la division cellulaire.
LA REPRODUCTION DE LA MOLÉCULE d’ADN.
Dans notre schéma 6, dans le haut, la molécule d’ADN est complète.
Dans le bas, les deux limons L1 et L2 commencent à se séparer par rupture des liaisons hydrogène des bases. La molécule se dégrafe comme dans une fermeture éclair.
Les nucléotides qui ont pu se détacher flottent dans le noyau et commencent à converger vers les deux limons écartés. Ils s’unissent à la base complémentaire :
T pour A
A pour T
G pour C
C pour G
Ainsi s’amorce la formation de deux échelles qui deviendront indépendantes dès que le dégrafage aura été total dans la molécule initiale.
Je cite au sujet de cette « réplication » un texte de J. RUFFIE (Traité du Vivant, page 227) :
« Lorsqu’une chaîne doit se reproduire … la double hélice (dont nous allons parler) se despirale puis s’ouvre par rupture des liaisons hydrogène qui unissent les bases puriques et pyrimidiques constituant les barreaux de l’échelle. Les barreaux ainsi coupés, les deux montants de l’échelle s’écartent, formant ainsi deux chaînes indépendantes, auxquelles restent attachés des hémi-barreaux …
Sous l’effet d’un système enzymatique complexe … chaque chaîne ainsi isolée provoque la synthèse d’une chaîne complémentaire. Cette synthèse débute par la partie de la double hélice qui s’est ouverte en premier et chemine de proche en proche. Finalement, l’on obtient deux hélices identiques à l’hélice primitive … »
Ainsi, seule la moitié des chaînes est de formation nouvelle ; la moitié initiale sert de matrice à la moitié de néo-formation.
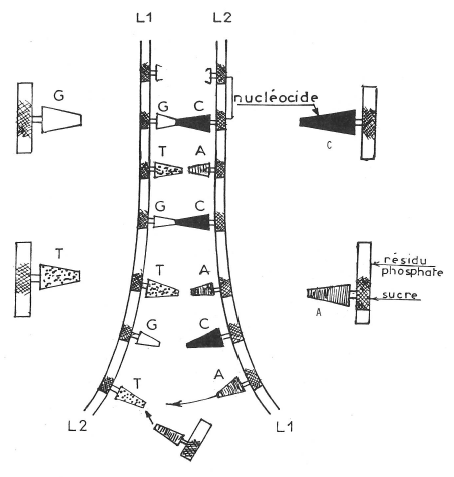
Fig. 6. Écartement des deux lignes et « réparation des dégâts ».
Réplication de la molécule d’ADN
2. – Structure secondaire.
Mais la molécule d’ADN n’est pas rectiligne.
Elle ressemble à une échelle de deux cordes, avec ses barreaux, tordue autour d’un axe imaginaire.
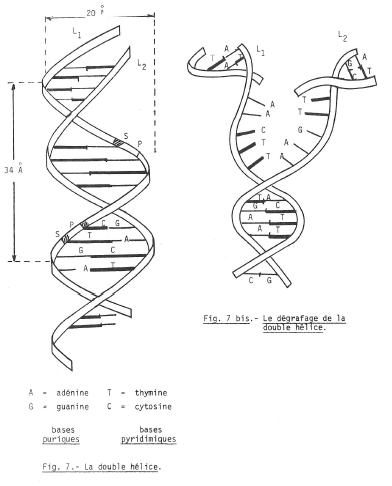
Il en résulte que les deux cordes forment une double hélice, d’une régularité singulière (fig. 7).
L’ensemble sucre et résidu phosphate forme ce qu’on appelle un nucléotide.
Or, tous les dix nucléotides, l’hélice fait un tour complet le pas en est de :

Comme chaque nucléotide porte un barreau, la distance entre deux barreaux est ainsi de :
34/10 = 3,4 Angström.
Quant à la distance qui sépare les deux limons, elle est de l’ordre de 20 Angström.
Ce schéma de la double hélice, confirmé en 1953 par Watson et Crick, après un fameux bricolage qu’ils décrivent dans « La double hélice », depuis 30 ans est toujours vrai pour l’essentiel ; il n’a subi que des retouches mineures.
Le schéma 7 bis montre le dégrafage de la double hélice.
Il semble y avoir une certaine relation entre la quantité d’ADN d’un organisme vivant et la complexité de ce dernier. C’est ce que montre le tableau suivant qui n’a qu’une valeur indicative sur la longueur et le nombre de barreaux.
| Quelques données numériques sur la molécule d’ADN | |
| Longueur d’un filament d’ADN dans une cellule |
Nombre de barreaux dans ce filament |
| Virus : 0,0127 mm | 170 000 |
| Bactérie : 0,1 mm | 7 000 000 |
| Étoile de mer : 30 cm | |
| Oiseau : 60 cm | |
| Homme : 90 cm | 6 000 000 000 |
| Grenouille : 240 cm | |
Ce qui est certain c’est qu’une seule erreur dans un barreau, un QC à la place d’un AT dans l’un des 6 000 000 000 de barreaux chez l’Homme peut donner naissance à un Homme anormal.
Enfin, on sait aujourd’hui que l’unité d’information n’est pas désignée par un seul barreau mais par trois barreaux successifs (triplet).
On peut alors aisément démontrer que si on prend 10 barreaux, le nombre des combinaisons possibles (donc les variations de l’information) sera de :
410/3 = 1048574/3 = 349524
Et comme la molécule chez l’Homme a 6 000 000 000 de barreaux, le nombre des combinaisons est de :
4 6 000 000 000/3
Que quelqu’un fasse le calcul !
LES PROTIDES.
Avec les protides, la question se complique singulièrement.
Le type mème des protides est le blanc d’œuf (ovalbumine).
Les protides sont des composés quaternaires qui contiennent carbone (C), hydrogène (H), Oxygène (O), azote (N).
Tous les êtres vivants, animaux et végétaux, en sont composés.
On peut classer les protides en trois groupes :
- les acides aminés,
- les polypeptides,
- les protéides.
Les acides aminés.
Ce sont des corps relativement simples formés
1) d’une partie invariante comprenant :
- un carbone central,
- sur lequel sont fixés :
- un atome d’hydrogène,
- une fonction acide caractérisée par le groupement-COOH,
- une fonction amine caractérisée par le groupement -NH2
2) d’une partie variable, le radical R qui permet de distinguer les acides aminés les uns des autres.
La formule générale d’un acide aminé est donc (fig. 8a)
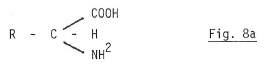
Chez les êtres vivants, du plus simple au plus complexe, on ne connait que 20 acides aminés alors que le nombre théorique possible est considérable.
Voici les formules de deux d’entre eux pris parmi les 20 (fig. Bb) :
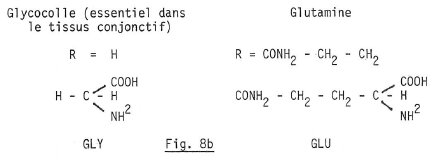
La grande propriété des acides aminés est que les molécules peuvent s’accrocher les unes aux autres par condensation entre le groupement COOH de l’un et le groupement NH2 de l’autre (fig. 8c). Ainsi se forment les longues des polypeptides.
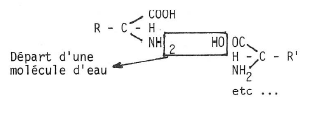
Fig. 8c Formation d’une liaison peptidique entre deux acides aminés.
La masse moléculaire des acides aminés ne dépasse pas 400 ; leur molécule est petite.
Les polypeptides :
Ils résultent de l’assemblage de plusieurs molécules d’acides aminés. Leurs masses moléculaires sont beaucoup plus élevées
- Lactalbumine 17 500
- Ovalbumine 38 000
- Hémoglobine du cheval 69 000
- Hémocyanine de l’escargot 5 000 000
Les protéides (ou protéines) sont de grosses molécules dont la masse moléculaire peut atteindre plusieurs millions.
Les acides aminés s’y trouvent en chaînes droites, ramifiées, à plat, en globes … (fig. 9).
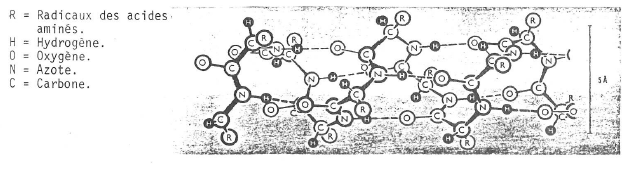
Fig. 9. Configuration hélicoïdale des chaînes polypeptidiques dans une protéine fibrillaire,
la kératine, qui constitue les cheveux, les ongles
Les protéides sont nombreux ; citons :
- kératine des poils, des ongles, des cornes,
- nucléoprotéines qui forment la masse principale des noyaux cellulaires,
- hémoglobine (qui renferme du fer) du sang,
- fibrinogène (du sang).
Formation des protides.
La question est trop complexe pour que nous l’abordions ici.
Je dis simplement : l’ADN dirige la synthèse d’une protéide en utilisant son code génétique : les barreaux formés des quatre bases A, T, G, C, placés dans un certain ordre, vont opérer la synthèse d’une protéine caractérisée par la nature et l’ordre des acides aminés qui la constituent.
Une cellule puise dans le sang les 20 acides aminés dont elle a besoin et qui proviennent de la digestion des aliments.
L’ADN du noyau de la cellule va envoyer au cytoplasme de cette cellule les informations nécessaires que ces acides aminés soient choisis et liés entre eux dans l’ordre requis pour édifier une certaine protéine.
Dans cette synthèse interviennent l’ARN-messager (dont nous ne parlerons pas) et les ribosomes signalés par Madame MARIOTTI lors de sa conférence sur la cellule.
CONCLUSION.
L’hérédité apparaît donc liée essentiellement à l’ADN.
Le code génétique est universel on le retrouve identique dans toutes les espèces vivantes, des bactéries à l’Homme.
Pour un fragment d’ADN donné c’est toujours la même synthèse qui est obtenue, même protéine et même enzyme, quelle que soit la catégorie de la cellule réceptrice.
Quatre bases : A, T, G, C.
Vingt acides aminés.
Voilà pourrait-on dire ce qui est commun, et ce qui fait un être vivant.
Mais quelle est l’origine de ce code universel ? il est difficile de répondre à la question ne serait-ce que parce que les fossiles prébiotiques n’ont laissé aucune trace dans les couches géologiques.
On peut dire – mais ce n’est pas une réponse – que l’origine du code se confond avec l’origine de la vie.
La génétique nous fait pénétrer dans les mécanismes de la vie au niveau moléculaire, mécanismes communs à tous les êtres vivants « de la bactérie à l’éléphant » (J. Monod).
Mais, comment une bactérie plutôt qu’un éléphant ou une souris plutôt qu’un homme ?
Si les recherches génétiques sont, semble-t-il, dans la bonne voie, la voie est encore longue à parcourir, mais elle est riche de promesses.
On est toutefois « émerveillé » par les acquises par les travaux qui datent d’un demi-siècle seulement et qui ont valu huit prix Nobel :
- 1833 – Th. H. Morgan – rôle des chromosomes dans l’hérédité.
- 1946 – H. J. Muller – Production de mutations sous l’influence des Rayons X.
- 1957 – Alexander Todd – Structure des acides nucléiques.
- 1958 – Beadle. Tatum, Lederber – Correspondance : un une enzyme.
- 1959 – Ochoa -Kurnberg – Synthèse d’ADN et d’ARN in vitro par polymérisation de nucléotides sous l’action d’enzymes extraites de bactéries.
- 1962 – Wilkins, Crick et Watson – structure hélicoïdale de la molécule d’ADN.
- 1965 – Lwoff, Monos. Jacob – Découverte de l’ARN-Messager – Régulation génétique de la synthèse des enzymes.
- 1968 – Niremberg, Holley, Khorana – Code génétique.
NOTE COMPLÉMENTAIRE SUR L’A.R.N.
Pour ne pas m’engager dans des problèmes de plus en plus complexes, j’avais décidé de limiter à l’A.D.N.
Mais voilà : à l’issue de la conférence sur la Région méditerranéenne une adhérente est venue me trouver pour me demander des renseignements qu’elle ne trouvait pas sur l’A.R.N., alors que rien ne lui manquait sur l’A.D.N.
Ce que je puis dire se limite à ceci :
D’abord les noms :
- A.D.N. = acide désoxyribonucléique,
- A.R.N. = acide ribonucléique.
Les différences entre A.D.N. et A.R.N.
Elles sont au nombre de deux :
- Dans les nucléotides de l’A.D.N. le sucre est le désoxyribose (fig. 1) tandis que dans l’A.R.N. le sucre est le ribose qui renferme un atome de plus d’oxygène (fig. 2).
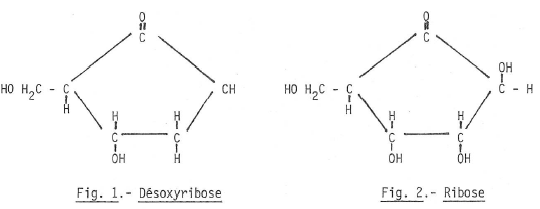
- A cette première différence s’en ajoute une seconde.
Les bases qui forment les barreaux sont toujours au de 4, mais la thymine (T) est remplacée par une autre base pyridimique = l’uracile (U).
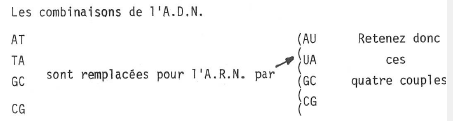
La formule d’un nucléotide de l’A.R.N., avec la base uracile, devient donc (fig. 3) :
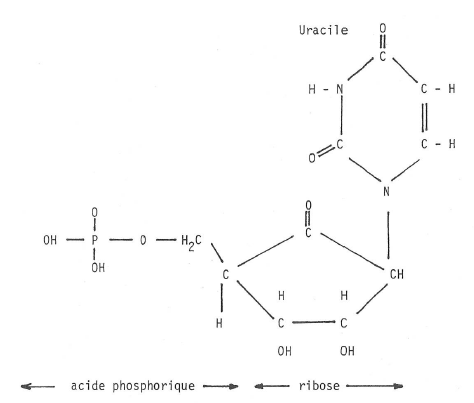
Fig. 3.-Uridine monophosphate
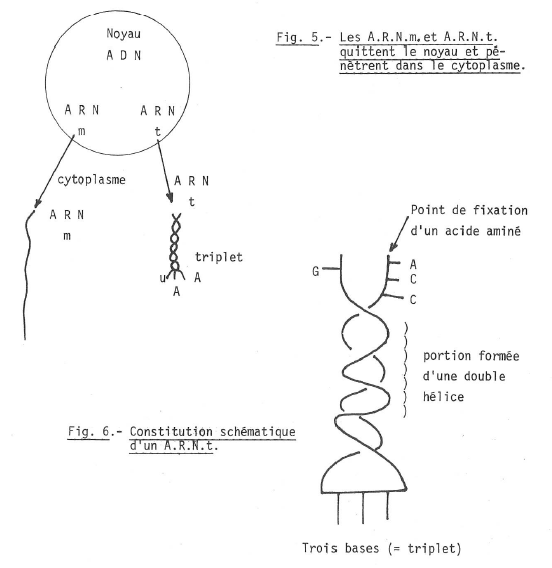
Les types d’A.R.N.
Parmi tous les types d’A.R.N. nous en retiendrons deux.
- les A.R.N. messagers (A.R.N.m) dont la dénomination est en rapport avec leur rôle ; leur molécule est une simple longue chaine non ramifiée. Ce sont les vecteurs du code génétique d’information et servent à la synthèse des protéines spécifiques au niveau des ribosomes ; ils disparaissent aussitôt leur message transmis.
- les A.R.N. de transfert (A.R.N.t). La molécule est courte, avec seulement environ 80 nucléotides sur une chaîne unique repliée sur elle-même en épingle à cheveu ce qui aboutit à une double hélice.
Ils servent à transporter les acides aminés au cours de la synthèse des protéines. Pour chaque acide aminé il y aurait un A.R.N.t spécifique.
A son extrémité l’A.R.N.t se termine par un triplet de bases, par exemple : U.A.A. – C.U.C. – A.A.A. – G.C.A.
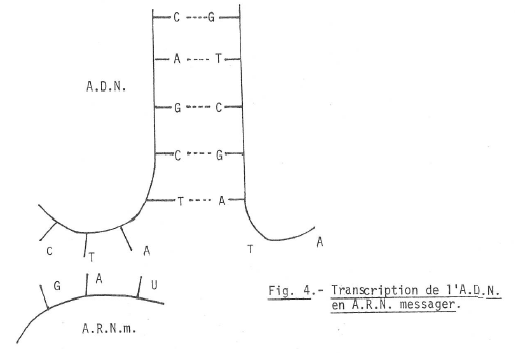
La transcription de l’A.D.N. en A.R.N.m.
Comment expliquer le transfert de l’information portée par l’A.D.N. à l’A.R.N.m ?
Les nucléotides des A.R.N.m s’appliqueraient le long de l’une des chaînes (un limon) momentanément dégrafée de l’autre (fig. 4). Il y aurait une sorte de moulage de l’A.R.N. à partir de l’A.D.N. servant de matrice.
Ce moulage se fait dans le noyau de la cellule.
La synthèse des protéines.
Une molécule de protéine est déterminée par la nature et l’ordre des acides aminés qui la composent. Ces acides aminés, qui proviennent de la digestion aliments, sont dans le cytoplasme de la cellule.
Le problème est le suivant = comment le noyau envoyer dans le cytoplasme les informations qui feront que ces acides aminés seront choisis et assembler entre eux dans un ordre déterminé et aboutiront ainsi à telle protéine plutôt qu’à une autre ?
La migration des A.R.N. dans le cytoplasme.
Les A.R.N. quittent le noyau en passa nt par les pores de la membrane nucléaire (fig. 5).
La synthèse des protéines.
L’A.R.N.m. gagne un ribosome (élément du cytoplasme) avec le moulage du code génétique) (fig. 7).
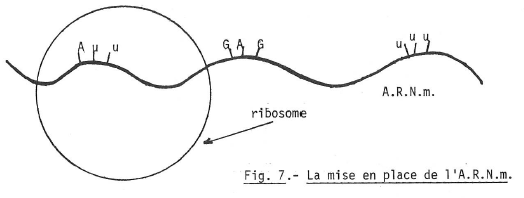
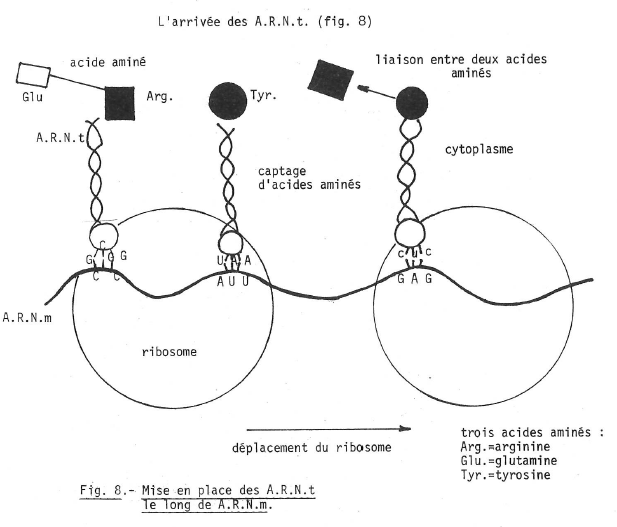
Chaque A.R.N.t capte, dans le cytoplasme, et suivant sa composition, un acide aminé déterminé.
Puis, à l’intérieur d’un ribosome, il va s’agrafer, avec son triplet de bases, à un triplet de l’A.R.N. messager, suivant l’association des Bases :
A avec U
U avec A
C avec G
G avec C
Ceci conduit à la mise en place d’un acide aminé.
Comme le ribosome se déplace le long de l’A.R.N.m., les A.R.N.t. agissent comme des ouvriers le long d’une chaine de montage. Les acides aminés, grâce à l’A.R.N.m., ont donc une place fixe les uns par rapport aux autres.
Dans un dernier temps, il y aurait combinaison entre eux des divers acides aminés, placés au voisinage les uns des autres, ce qui, du même coup, libère les triplets de transfert qui peuvent ainsi intervenir de nouveau. La libération d’un A.R.N.t. est le signal d’un glissement relatif du ribosome et de l’A.R.N.m.
La chaine d’acides aminés s’accroit et se transforme en molécule de protéine qui finit, elle aussi, par être libérée.
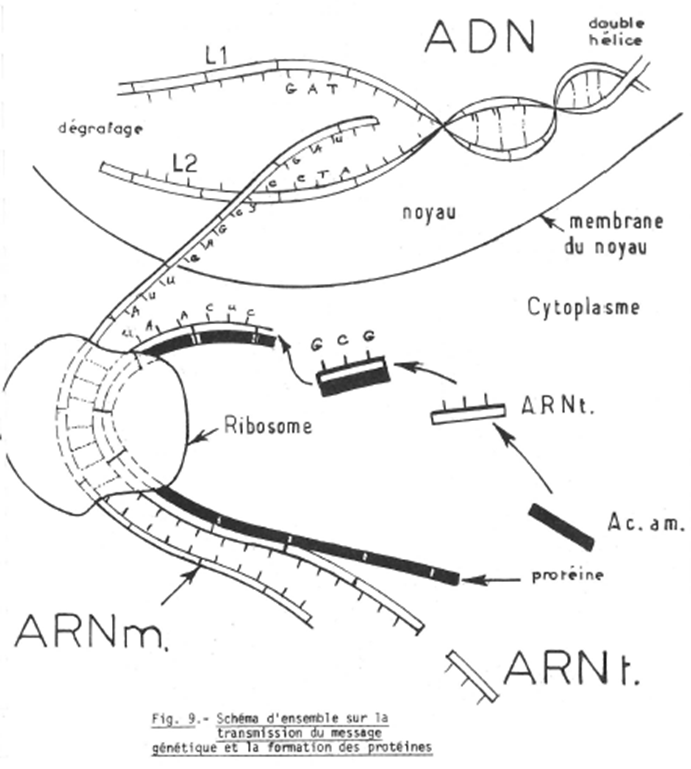
Le schéma ci-joint (fig. 9) donne une vue d’ensemble sur la transmission du message génétique et la formation des protéines.
Dans le noyau de la cellule = la double hélice de l’A.D.N.
La longue molécule.de l’A.D.N. est constituée par deux brins (L1 – L2) qui s’enroulent l’un autour de l’autre en formant une double ; les brins sont réunis par des bases qui sont comme des barreaux d’une échelle ; nous avons désigné ces barreaux par 4 lettres A, T, G, C, assemblées de la sorte AT, TA, GC, CG.
A.R.N. messager (A.R.N.m) et A.R.N. de transfert (A.R.N.t).
- Les protéines sont fabriquées par la cellule selon les instructions contenues dans l’A.D.N. Les instructions doivent quitter le noyau et passer dans le cytoplasme.
Le mécanisme est le suivant = les deux limons L1 L2 de l’A.D.N. se dégrafent ; dans l’ouverture le brin d’A.R.N. vient prendre des instructions sur un limon de l’A. D. N.
L’A.R.N. est donc chargé d’une « copie complémentaire » de l’un des deux brins de l’A.D.N.
Il quitte le noyau et pénètre dans le cytoplasme avec le message génétique ; d’où son nom d’A.R.N. messager.
D’autres chaînes d’A.R.N., plus courtes, quittent également le noyau ; ce sont les A.R.N. de transfert dont nous allons voir le rôle.
- Rôle du ribosome dans la formation des protéines.
Le ribosome est une sorte de moule ; y entrent l’A.R.N. messager et les A.R.N. de transfert dont chacun porte son acide aminé, élément constitutif des protéines.
Sort du ribosome une longue chaine d’acides aminés, assemblés l’un après l’autre, dans l’ordre fixé par le code génétique. Ayant lâché son acide aminé, l’A.R.N. de transfert est libéré et part se recharger dans le cytoplasme.
L’A.R.N. de transfert est bien l’adaptateur qui suit les instructions de l’A.R.N. messager qui, lui-même, est la copie complémentaire de l’A.D.N.
La protéine se construit donc avec des acides aminés, choisis et assemblés dans un ordre déterminé par le code génétique.
Découvrez + de 1100 textes des conférences du CDI sur le site du CDI de Garches
Vos commentaires et vos conseils contribuent à l’amélioration de nos parutions.
Vous disposez de l’espace « COMMENTAIRES » ci-dessous pour les exprimer.
Merci et à bientôt pour votre prochaine visite.

Laisser un commentaire