Thèmes : sciences.
Conférence du mardi 5 février 1980.
Le mardi 5 février, Monsieur GINOT, physicien, adjoint au chef du département des relations publiques au Commissariat à l’énergie atomique, fit un exposé, très apprécié d’un nombreux public, sur la « radioactivité à votre service ».
En quelques mots, Monsieur SIRE rattacha cet exposé à celui de Monsieur Pierre LEVEQUE sur l’énergie nucléaire et la production d’électricité, et marqua la différence entre la fission de l’atome qui produit de l’énergie et la désintégration spontanée du noyau de l’atome qui s’accompagne de l’émission de radiations de plusieurs types.
L’exposé de Monsieur GINOT, particulièrement riche et toujours très clair et très alerte, fut introduit par la projection d’un film hautement pédagogique, au titre évocateur « les Instables » ; pourquoi certains noyaux d’atomes sont-ils bien solides alors que d’autres, les Instables, sont instables ? Le film apportait une réponse à ces questions.
Sur 325 noyaux naturels, 274 sont stables ; tous les autres sont instables. Mais l’homme a su agir sur les noyaux naturels et les transmuter en un grand nombre de types nouveaux d’atomes ; on en connait aujourd’hui plus de 1500 qui tous sont instables.
Monsieur GINOT donne des exemples de noyaux stables :
- le nickel : 28 protons et 32 neutrons : 60 nucléons
- le néon : 10 protons et 10 neutrons : 20 nucléons
- le mercure : 80 protons et 120 neutrons : 200 nucléons
- l’or : 79 protons et 118 neutrons : 197 nucléons
mais au-delà de 209 nucléons, les noyaux deviennent instables à cause d’un excédent de neutrons ; ainsi :
- le polonium : 84 protons + 126 neutrons : 210 nucléons
- l’uranium : 92 protons + 143 neutrons : 235 nucléons
- le plutonium : 94 protons + 148 neutrons : 242 nucléons
- le bismuth est la limite : 83 protons + 126 neutrons : 209 nucléons
Monsieur GINOT peut alors aborder la question des isotopes qui, pour un même élément, ont dans leur noyau toujours le même nombre de protons :
exemple : l’oxygène a trois isotopes
- 8 protons + 8 neutrons : 16 nucléons
- 8 protons + 9 neutrons : 17 nucléons
- 8 protons + 10 neutrons : 18 nucléons
Le carbone 12 a
- 6 protons + 6 neutrons : 12 nucléons
- 6 protons + 7 neutrons 13 nucléons
Le carbone 14 a
- 6 protons + 8 neutrons : carbone 14 radioactif
Les « Instables » ont la propriété de se désintégrer, c’est-à-dire de voir brutalement et spontanément leur structure se modifier en éjectant des radiations : c’est cette émission de radiations qui constitue la radioactivité. Tout se passe comme le noyau, par ces éjections, cherchait à trouver une forme stable.
Monsieur GINOT a beaucoup insisté sur l’indépendance des phénomènes de radioactivité vis-à-vis de la température, de la pression, des réactions chimiques dans lesquels interviennent les atomes radioactifs. C’est grâce à cette indépendance que les éléments radioactifs peuvent être utilisés comme traceurs dans l’organisme.
Leur vie (qui correspond la période la moitié de leur masse) est plus ou moins longue :
| Carbone 14 | : 5700 ans |
| Radium 226 | : 1526 ans |
| Uranium 238 | : 4,5 milliards d’années |
D’autres ne vivent que quelques secondes.
La détection des radiations se fait par :
- la plaque photographique
- les compteurs (Geiger)
- la scintillation (celle des cadrans de nos montres)
- les chambres de Wilson ou à bulles
Les désintégrations font que l’on passe d’un élément à un autre ; ainsi du polonium 210 (84 + 126) par désintégrations successives, on arrive au plomb stable 206 (82 + 124), au rythme de 12,6 milliards de désintégrations par seconde.
TROIS TYPES FONDAMENTAUX DE RADIATIONS (fig. 13)
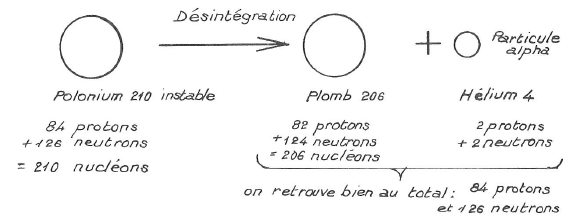
- Rayonnement alpha : il est constitué de particules qui sont de véritables noyaux d’hélium (2 protons + 2 neutrons) chargés positivement
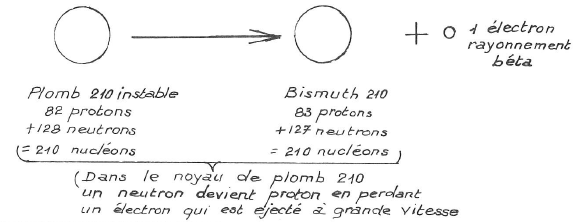
- Rayonnement bêta : formé d’électrons chargés négativement (on parle alors de rayonnement bêta moins)
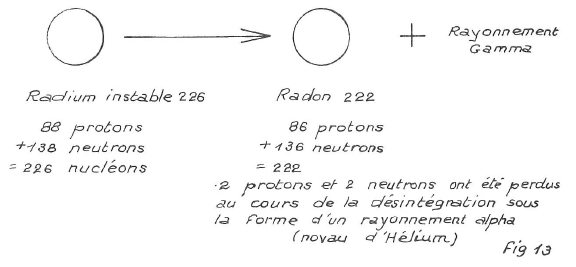
- Rayonnement gamma : dépourvu de charge et de masse ; c’est un rayonnement électromagnétique, comme la lumière et les rayons X, qui se propage à la vitesse de la lumière.
On a mis en évidence un rayonnement bêta plus formé de positons qui sont les antiparticules des électrons négatifs ; pour son émission, un proton se transforme en un neutron avec éjection d’un électron positif.
C’est le du phosphore 30 : 15 protons + 15 neutrons : 30 nucléons en perdant un proton devient 14 protons (15-1) + (15+1) neutrons = 30 nucléons soit le silicium stable avec éjection d’un positon bêta plus.
Nous sommes contraints d’abréger le compte-rendu et de citer rapidement les applications de la radioactivité :
- l’horloge atomique qui utilise la longueur d’onde de 3,3 cm émise par le césium 133 et dont la variation est de 1 seconde en 3000 ans.
- les applications médicales : dosage des hormones, dépistage et traitement des tumeurs (bombe au cobalt), les traceurs et les indicateurs.
- la datation des roches et des fossiles en particulier par le carbone 14.
- la gammagraphie des pièces métalliques pour vérifier par exemple les soudures.
- la stérilisation par les rayons gamma des conserves, du lait, des viandes… de la momie de Ramsès II.
- les mutations volontaires de plantes par les horticulteurs : petits pois plus résistants aux maladies, pailles de blé plus dures et plus faciles à couper par les faucheuses.
- la mesure de l’épaisseur de la couche de bitume déposée sur la route.
- etc.
L’exposé de Monsieur GINOT était accompagné de la projection de diapositives. Les auditeurs ont pu « entendre » grâce à un compteur Geiger, les radiations émises par un minerai d’uranium. La séance s’est terminée par projection d’un beau film « Nucléart » sur la restauration des œuvres d’art par application de la radioactivité.
LA RADIOACTIVITÉ
DESINTEGRATION ALPHA
DESINTEGRATION BÊTA
RAYONNEMENT GAMMA (schéma très simplifié)
Découvrez + de 1100 textes des conférences du CDI sur le site du CDI de Garches
Vos commentaires et vos conseils contribuent à l’amélioration de nos parutions.
Vous disposez de l’espace « COMMENTAIRES » ci-dessous pour les exprimer.
Merci et à bientôt pour votre prochaine visite.

Laisser un commentaire