Thèmes : médecine, sciences.
Conférence du mardi 30 novembre 1982.
En manière d’introduction.
Ces quatre photographies remarquables, prises au microscope électronique à balayage, concernent l’épithélium de la trachée du Furet (Fig. 1).
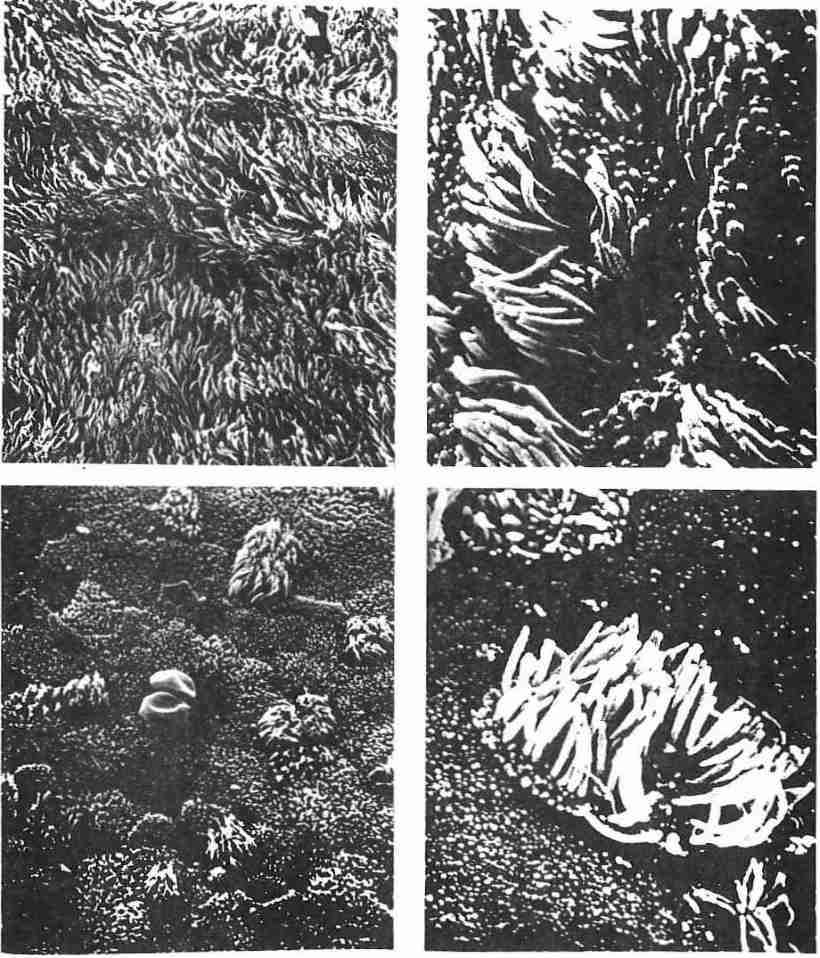
Fig. 1.
- Le Furet est sain ; on distingue nettement les cils vibratiles des cellules de l’épithélium qui tapisse l’intérieur de la trachée.
- Photographie de mème signification à un plus fort grossissement.
- Le Furet est atteint par le virus de la grippe ; le virus provoque localement la disparition des cils en l’espace de 24 heures environ et laisse l’épithélium complètement « pelé ».
- Puis, progressivement, les cils régénèrent.
Cet épithélium est cilié, les cils étant les prolongements cytoplasmiques, extrêmement fins et petits, des cellules qui tapissent l’intérieur de la trachée ; ces cils sont vibratiles (fig. 2).
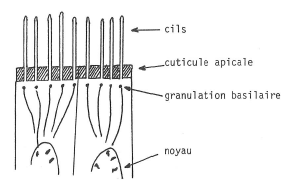
Fig. 2. Deux cellules ciliées de l’épithélium de la trachée.
Le mardi 30 novembre, Monsieur BARME, professeur à l’Institut Pasteur, chef de service de virologie médicale, entretenu une nombreuse assistance des « vaccins contre les maladies à virus ».
I. LES ACTEURS : LES VIRUS.
Une première diapositive montre une préparation au microscope électronique dans laquelle se trouvent des rotavirus. Ils ont un aspect caractéristique évoquant une roue (latin : rota) d’où le nom donné à ces virus.
Les rotavirus sont responsables d’un grand nombre d’affections diarrhéiques chez l’enfant et chez diverses espèces de Mammifères (fig. 3).
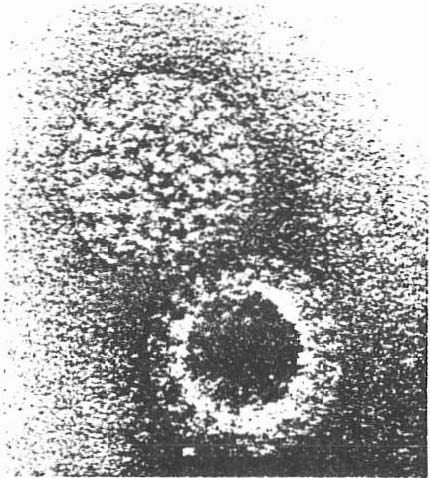
Fig. 3. Les rotavirus mesurent 67nm et sont dépourvus d’enveloppe.
Sur une autre diapositive nous voyons le virus de la grippe (fig. 4). Il est très polymorphe et revêt des formes sphériques, allongées, filamenteuses. On distingue une enveloppe.
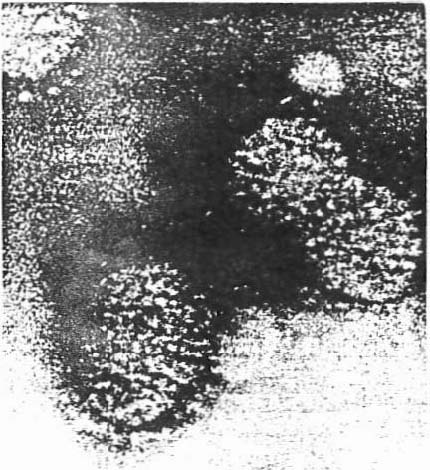
Fig. 4.
Morphologiquement, les virus se distinguent par différents caractères tels que la taille, le matériel génétique (RNA ou DNA), la présence ou non d’une enveloppe, etc. Par exemple, le virus de la grippe est un virus RNA qui mesure 90 à 120nm de diamètre et possède une enveloppe. Sa transmission se fait par voie aérienne et les virus-semblent mieux se conserver en atmosphère relativement sèche.
La taille.
Les virus sont des particules très petites dont la taille exige l’emploi du microscope électronique avec des grossissements qui atteignent 500 000.
Pour mesurer leur diamètre on utilise comme unité de longueur le nanomètre.
Le virus de la polio a un diamètre de 22 à 24 nm, celui de la grippe de 90 à 120 nm, celui de la psittacose 270 nm.
Les figures 5 et 6 donnent le schéma de deux types de virus, nu et à enveloppe.
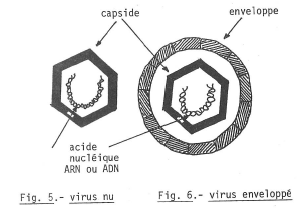
Le parasitisme total.
Ils ne peuvent se multiplier qu’à l’intérieur d’une cellule vivante.
Pour cela ils vont pénétrer dans des cellules, détourner le fonctionnement de la cellule de telle sorte qu’au lieu de fabriquer du matériel cellulaire, la cellule parasitée va se mettre à fabriquer du virus.
Ce parasitisme est dû à la présence d’un acide nucléique à l’intérieur de la particule virale (A.D.N. : acide désoxyribonucléique, A.R.N. : acide ribonucléique) (fig. 7).
Les cellules animales normales disposent des 2 acides nucléiques.
Les virus ont soit l’un, soit l’autre. C’est pour cela qu’ils doivent parasiter une cellule vivante.
Les bactéries se distinguent des virus par beaucoup de caractères et en particulier dans le domaine de la reproduction, par le fait qu’elles se multiplient très bien sur des milieux de culture (exemple : gélose), genre de culture impossible avec les virus.
La structure.
On connaît maintenant la structure fine de la plupart des espèces virales. Une particule virale a une structure rigide à symétrie cubique : il s’agit le plus souvent d’un isocaèdre, c’est-à-dire d’un polyèdre à 20 faces semblables (fig. 8) qui sont des triangles équilatéraux, de 12 sommets et de 30 arêtes.
D’autres symétries sont possibles, en particulier la symétrie hélicoïdale ; c’est le cas du virus de la mosaïque du Tabac (voir annexe).
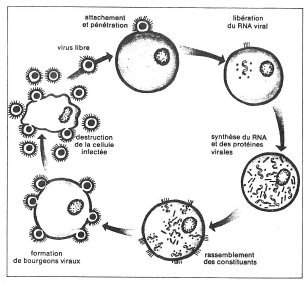
Fig. 7. Les virus ne sont capables de se multiplier qu’au sein de cellules vivantes dont ils provoquent le plus souvent la destruction. Ce schéma représente le cycle très simplifié du virus de la grippe. Les virus sont équipés de molécules superficielles (glycoprotéines) douées d’affinité pour les membranes des cellules leur permettant de s’attacher et.de pénétrer. Le virus libère ensuite sa nucléocapside, c’est-à-dire son matériel génétique (qui est dans ce cas-là du RNA) associé à une protéine, tandis que l’enveloppe virale fusionne avec la membrane de la cellule. Puis, par un processus complexe, l’acide nucléique viral libéré oriente la cellule dans un sens anormal qui lui permet de se reproduire et de détourner la machinerie cellulaire à son profit pour lui faire produire les protéines virales plutôt que les protéines cellulaires. Acides nucléiques et protéines virales nouvellement synthétisés s’associent pour former des nucléocapsides. En mème temps, d’autres protéines virales (glycoprotéines) se placent à certains endroits de la surface de la membrane cellulaire. Les nucléocapsides viennent ensuite se rassembler à ce niveau de la membrane cellulaire et amorcent un processus de bourgeonnement. Les virus ainsi formés sont libérés dans le milieu extra-cellulaire, entraînant progressivement la destruction de la cellule hôte.
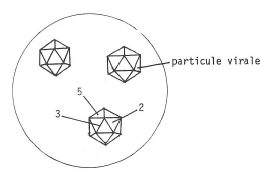
Fig. 8. Icosaèdre constitué de 12 sommets d’ordre 5
(5 triangles équilatéraux y aboutissent, chaque triangle aboutissant à 3 sommets),
de 20 faces et de 30 arêtes. Un tel solide possède trois axes de symétrie 5,3.2.
Autour de cette forme géométrique parfaite qui représente une boîte appelée capside, se trouvent les capsomères constitués de protéines (fig. 9).
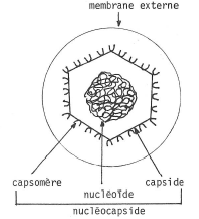
Fig. 9. Schéma du virus Herpétique et de ses constituants.
II. LES VACCINS.
L’histoire a retenu les noms de Jenner qui utilisa, en 1796, le virus d’une maladie animale, la vaccine (fig. 10) pour protéger l’Homme contre la variole ; et celui de Pasteur qui fournit, cent ans plus tard, une base scientifique à la préparation de vaccins contre le charbon et contre la rage (1884).

Fig. 10. Virus de la vaccine
Les vaccins confèrent une immunité active, spécifique contre une maladie déterminée, par inoculation de l’agent pathogène atténué ou inactivé de cette maladie ou de sa toxine rendue inoffensive.
Il existe 2 variétés de vaccins :
- les vaccins à virus atténués ou vivants,
- les vaccins à virus inactivés ou tués.
1. Vaccins à virus atténués ou vivants.
Le virus vivant, injecté dans l’organisme, se multiplie. Il réalise une infection avec une production massive de particules virales filles. Cette multiplication se passe sans aucun symptôme clinique. Les virus, utilisés pour préparer ces vaccins, ont été sélectionnés pour la perte de leur pouvoir pathogène. Donc lorsqu’on vaccine avec un vaccin vivant, on introduit dans l’organisme simplement une dose infectante qui aboutit à une masse considérable de virus qui va provoquer à la fin de l’infection une immunité.
2. Les vaccins inactivés ou tués.
On part d’un matériel viral vivant en laboratoire soumis à l’action de différents agents, il est tué.
On a donc affaire à une dose de matériel viral inerte qui se comporte comme un agent chimique. Introduit dans l’organisme, par injection, il va provoquer une réaction de l’organisme pour constituer un état de protection.
On choisit le type de vaccin en fonction de la maladie et des souches de virus disponibles.
Actuellement, tous les vaccins sont préparés à partir de virus multipliés dans des cellules vivantes.
Préparation.
Pendant longtemps, on a préparé les vaccins en utilisant des animaux entiers. Pour la variole, on inoculait dans la peau de Bovidés ou de Moutons. Grâce à cette inoculation avec le virus de la vaccine, proche de celui de la variole, il se formait des pustules dans lesquelles se trouvait une très grande quantité de particules virales. L’animal étant sacrifié, il ne restait plus qu’à faire un raclage de la peau pour récupérer tous les virus produits à l’intérieur de ces pustules. A partir de cette suspension, on préparait les vaccins contre la variole.
Ce procédé posait un certain nombre de problèmes car dans ce liquide se trouvaient des substances étrangères.
D’autre part, s’adresser à des animaux comportait des risques car ils pouvaient être malades.
L’étape suivante fut le recours aux œufs de poule.
On place un œuf dans une couveuse ; on obtient ainsi un œuf embryonné (fig. 11).
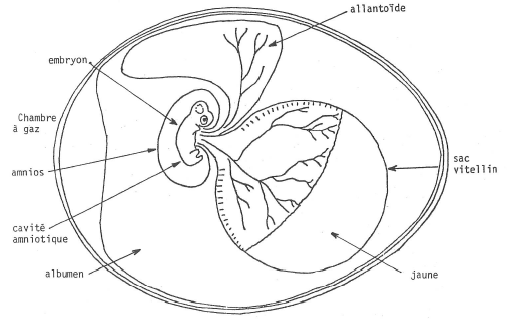
Fig. 11. Coupe schématisée d’un œuf de Poule à 10 jours d’incubation.
L’embryon est couché perpendiculairement à l’axe de l’œuf, sur le côté gauche, le dos vers le gros bout.
On introduit une petite quantité de virus dans la cavité allantoïdienne. Le virus pénètre dans les cellules, infecte l’embryon, la membrane amniotique et se multiplie. Au bout de quelques jours, on récolte le liquide allantoïdien (10cm3 par œuf environ) qui sert de matériel de départ pour le vaccin (grippe). Pour la fièvre jaune, on récolte l’embryon entier broyé. Mais l’œuf ne peut permettre la multiplication de toute espèce virale.
. Dans les années 50 on a découvert la possibilité de multiplier des virus sur cultures cellulaires. Le premier vaccin contre les maladies virales préparé sur des cultures cellulaires a été celui de la poliomyélite (1954 Salk).
Un tel vaccin se fait sur des cellules en culture primaire.
On part des reins de singe que l’on coupe en petits morceaux.
Ils sont soumis à un enzyme qui rompt les liaisons inter-cellulaires. On aboutit ainsi à une suspension de cellules rénales séparées. Elle est remise en suspension dans un milieu de culture spécial qui permet aux cellules de se fixer sur la paroi du récipient dans lequel on fait la culture. Les cellules peuvent ainsi se diviser et se multiplier. On obtient alors une couche monocellulaire de cellules vivantes.
Les cellules de reins de singes sont sensibles au virus de la polio qui va pouvoir y pénétrer et se multiplier.
On pourra ainsi récolter des quantités énormes de virus vivants de la poliomyélite.
Le recours aux cultures cellulaires primaires représentait un très grand progrès ; mais ces cultures sont source d’inconvénients :
- il faut pour chaque lot de vaccins tuer des singes,
- ces singes venant de la brousse portent en eux des virus dont certains sont dangereux pour l’Homme.
Ces virus contaminants se retrouvent dans les cellules en culture et se mélangent au virus de la polio de sorte que l’on doit faire des quantités de contrôles pour s’assurer de l’absence de ces virus étrangers.
On a donc cherché d’autres procédés. On s’est alors tourné vers les cellules diploïdes (qui ont 2n chromosomes). Ce sont des cellules normales qui dérivent de tissus d’embryons qui se multiplient.
A partir de la culture primaire qui a fourni un tapis cellulaire complet, on effectue des passages de façon à entretenir la culture cellulaire.
On obtient une culture en lignée (jusqu’à 50 passages). A chaque passage on multiplie le nombre de cellules par 2. Donc, au bout de 50 passages, on a un nombre fantastique de cellules (250 = 1,12 x 1015)
Pour augmenter encore ce nombre de passages, on utilise des lignées cellulaires de cellules hétéroploïdes, c’est-à-dire qui montrent certaines transformations cellulaires.
On obtient ainsi des lignées permanentes. On peut entretenir indéfiniment ces cellules. De plus ces cultures sont beaucoup plus riches en cellules ce qui permet d’obtenir un plus grand nombre de particules virales.
On utilise les cultures permanentes uniquement pour les vaccins tués à une exception près : le vaccin contre l’hépatite virale B.
On n’a jamais pu multiplier ce virus dans des cultures cellulaires mais seulement chez l’Homme malade ou chez le chimpanzé. Pour ce cas particulier on prépare actuellement un vaccin à partir du sang de donneurs qui sont porteurs d’une infection chronique par le virus de l’hépatite B. Ils ont eu une hépatite, ont mais continuent à fabriquer des particules virales et un antigène Hbs. Ainsi on isole du plasma des porteurs sains, par purification chimique, la protéine vaccinante porteuse de l’antigène Hbs. Cette méthode est cependant appelée à être remplacée. En effet, d’une part la méthode de purification chimique a des limites ; la protéine porteuse du signal Hbs est en effet associée, dans l’enveloppe du virus, à des protéines de type albumine provenant de l’hôte et la purification chimique n’arrive qu’incomplètement à les séparer ; d’autre part le développement même de la vaccination risque de raréfier le nombre des porteurs sains, source de protéines vaccinantes.
Donc l’un des grands avantages du recours aux cultures cellulaires est de ne plus avoir besoin d’animaux. On dispose de cellules diploïdes ou permanentes, congelées sous forme de semences cellulaires, dans des réservoirs d’azote liquide à -194°C. Ainsi, les cellules restent indéfiniment vivantes.
4. Procédé de culture cellulaire.
Les méthodes de culture classiques n’exigent aucun appareillage compliqué.
On a souvent utilisé des flacons stationnaires, des bouteilles plates, placées horizontalement. Les cellules se déposent et forment un tapis continu sur le fond.
Une culture cellulaire s’exprime en surface de culture.
Pour fabriquer beaucoup de vaccins, on a cherché le moyen d’augmenter la surface cellulaire.
Pour cela on a utilisé des flacons cylindriques mis sur une machine tournante. Le flacon tournant, les cellules se déposent sur toute la surface interne du cylindre.
Actuellement le procédé le plus prometteur est la culture sur des micro supports en suspension. On utilise de petites sphères en matière plastique. Ces billes ont environ de diamètre ; elles sont mélangées avec une suspension de cellules qui se fixent à la surface des billes et se multiplient. La somme des surfaces des billes dans un récipient de dimension relativement réduite est très grande. Un fermenteur de 100 litres fournit autant de cellules que 5000 flacons de verre d’un litre.
Fabrication du virus.
La récolte de virus doit être traitée pour se transformer en vaccin :
- vaccin vivant : on purifie et on ajuste la teneur en particules virales vivantes pour faire une dose.
- vaccin tué : on fait agir sur la suspension virale récoltée, un agent d’inactivation qui tue le virus. On utilise le formol, le béta-propiolactone, le n butyl phosphate, la chaleur, les rayons U.V. Puis on purifie.
Les contrôles sont très difficiles et obligatoires. Chaque laboratoire doit tenir un registre. Si l’un des contrôles donne un résultat insatisfaisant, il faut jeter la totalité du lot de vaccins en préparation.
Le meilleur exemple de vaccin que l’on puisse citer est celui contre la variole.
La variole existait depuis des siècles. On a retrouvé dans un tombeau égyptien des traces de lésions de variole sur la peau d’un homme.
A la suite d’une campagne d’éradication menée par l’O.M.S. (Organisation Mondiale de la Santé), dans tous les pays du monde, le nombre de cas de variole a diminué de plus en plus jusqu’à une disparition totale. C’est en Somalie en octobre 1977 qu’on a relevé le dernier cas. On conserve des souches du virus de la variole dans 3 laboratoires de haute sécurité dont Atlanta et Johannesburg.
En ce qui concerne la poliomyélite, les U.S.A. comptaient 37000 cas entre 1951 et 1955 avant que le vaccin n’existât.
En 1955 commença la vaccination de masse qui fut suivie d’une chute importante du nombre de cas.
- En 1960, on dénombre 2500 cas,
- de 1962 à 1965, 573 cas (vaccin vivant),
- 1980, moins de 10 cas par année.
La rougeole.
On a commencé à vacciner en masse contre la rougeole en 1963 aux U.S.A. On estime que la rougeole est en voie de disparition.
Le virus est parfaitement adapté à l’Homme, qui peut constituer son unique réservoir dans la nature.
Le virus s’attaque essentiellement à l’appareil respiratoire du rhino-pharynx au poumon. L’inflammation qui en résulte expose cet appareil à de fréquentes surinfections bactériennes, la plus banale étant l’otite, la plus grave la bronchopneumonie.
Tout enfant n’est pas à l’abri d’une complication redoutable, échappant à toute prévision et à tout traitement, heureusement peu fréquente, due à l’agressivité particulière du virus pour le système nerveux : l’encéphalite.
Pour éliminer ces maladies, il faut d’abord s’attaquer aux maladies cibles, qui ne s’attaquent qu’à l’homme et pour lesquelles l’éradication est possible (oreillons, rougeole, rubéole, polio). La tâche est plus compliquée quand il existe un réservoir animal (rage, fièvre jaune).
6. L’avenir.
On continue à faire des recherches pour trouver le moyen de préparer des vaccins qui reviennent moins chers.
Actuellement 2 voies possibles existent. :
-
le recours au génie génétique (fig. 12)
La particule virale comprend une capside et un acide nucléique qui est un assemblage de gènes représentant le patrimoine héréditaire du virus. Chaque gène se comporte comme une instruction d’un programme d’ordinateur. Dans une particule virale complète il y a de nombreux constituants dont certains représentent le matériel immunogène, c’est-à-dire la matière qui possède la faculté d’induire un état de protection et qui vaccine. Cela peut être une partie de la particule, par exemple les spicules qui possèdent des glycoprotéines, qui possèdent eux-mêmes le pouvoir vaccinant. Donc tout le reste de la particule ne sert à rien.
Dans l’idéal, on pourrait faire un vaccin avec seulement les spicules. Or, dans l’acide nucléique du virus, il existe un gène qui code pour la fabrication des spicules.
Soit une cellule animale (fig. 13).
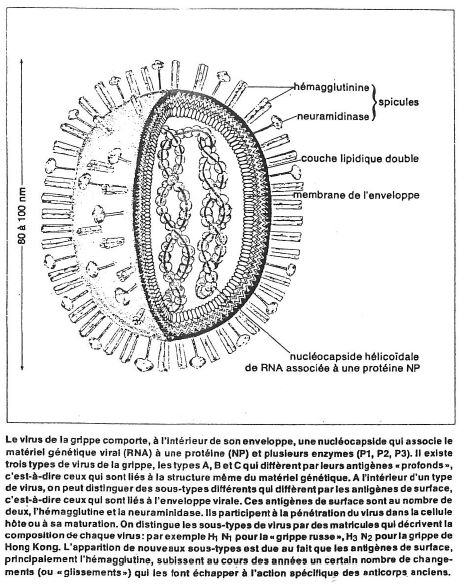
Fig. 12.
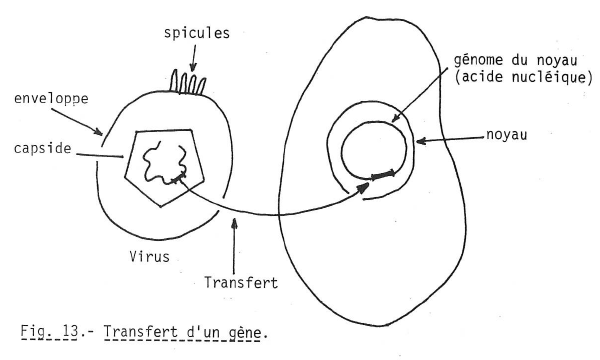
Par un procédé spécial, on prélève ce gène du virus qui code pour la fabrication des spicules et on l’introduit dans le génome. La cellule va fa briquer des spicules de virus.
« Il n’y aura plus qu’à » purifier ces spicules et préparer un vaccin.
-
voie de la synthèse.
Dans une particule virale, seules quelques fractions de la matière qui la compose possèdent la propriété de vacciner. Or, on sait aujourd’hui que l’assemblage d’une capside par exemple, qui représente la réunion de capsomères (des protéines composées de polypeptides), est un enchainement d’acides aminés, dont certains peuvent suffire porter le pouvoir vaccinant.
Des travaux de recherche sur la polio sont conduits dans le monde, visant connaître le nombre exact d’acides aminés capables de vacciner contre cette maladie.
Dans le cas de ce virus, l’icosaèdre est entouré de 5 faces, sur lesquelles se trouve 1 capsomère.
On peut en faire l’analyse par une électrophorèse dans un milieu gélifié en prenant un cylindre dans lequel on place un gel. Dans la partie supérieure on dépose une préparation des capsomères. On fait ensuite passer un courant électrique continu. En fonction de leur masse, et de leurs différentes caractéristiques physico-chimiques, les constituants protéiques des capsomères se séparent dans le gel. On voit apparaître alors des taches représentant un polypeptide séparé dont on connait la structure et le poids moléculaire. On les appelle VP (viral protéine) (fig. 14).
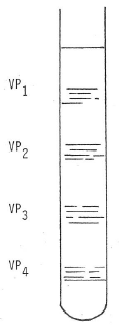
Fig. 14. Résultat d’une électrophorèse.
On a pu séparer ces protéines virales purifiées et les étudier. Le pouvoir vaccinant de la polio est porté uniquement par le VP1. On peut aller encore plus loin en disant que seuls certains acides aminés de ce polypeptide portent le pouvoir vaccinant.
Si l’on arrive identifier les acides aminés qui composent cette petite chaîne, partie du VP1, on peut fabriquer ces peptides par synthèse condition d’avoir reconstitué l’ordre des acides aminés dans ce fragment de chaîne. Mais pour qu’il soit fonctionnel et qu’il vaccine, il faut qu’il ait une certaine configuration dans l’espace. C’est tout le problème auquel se heurtent les chercheurs actuellement.
En résumé, sur la structure des virus il n’y a que quatre choses à retenir.
Dans sa petite taille de 150 à 200 nanomètres, les herpès virus sont composés :
- de protéines,
- d’acide désoxyribonucléique (ADN),
- d’une capside,
- et d’une enveloppe (fig. 15).
Le virus est formé de prismes hexagonaux et pentagonaux disposés suivant les axes de symétrie d’un isocaèdre.
Ces prismes, qui sont les capsomères, recouvrent la capside isocaédrique.
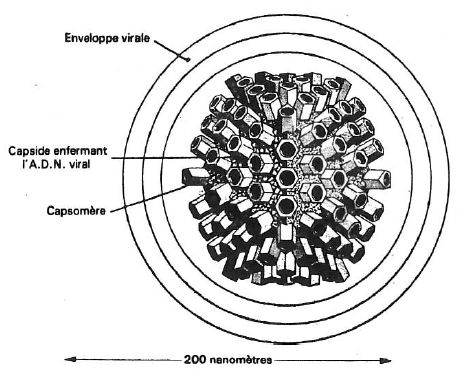
Fig. 15.
L’A.D.N. se présente sous la forme d’une double chaine qu’entoure une masse protéique.de forme cylindrique. Il permet, par son code génétique, la synthèse d’une soixantaine de protéines.
Il est enfermé dans la capside.
Celle-ci, de nature protéique, est un isocaèdre régulier de 20 faces, composée de 162 unités structurales ou capsomères.
Voici le décompte pour le virus herpétique :
- chacune des 20 faces de l’isocaèdre renferme 3 capsomères 20 x 2 : 60
- chacune des 30 arêtes, 3 30 x 3 : 90
- chacun des 12 angles, 1 12 x 1 : 12
=> TOTAL 162 capsomères
L’enveloppe est une dérivée de la membrane nucléaire de la cellule infectée ; le virus l’acquiert par « bourgeonnement » au moment où il sort du noyau de cette cellule. L’enveloppe est composée de trois feuillets.
La section plane d’un isocaèdre est rigoureusement pentagonale (ou hexagonale) (fig. 16).
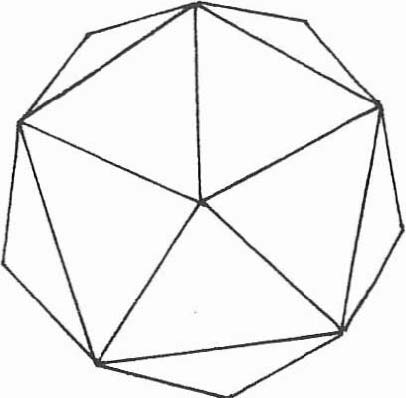
Fig. 16
ANNEXE 1
La mosaïque du Tabac et la structure hélicoïdale (fi g. 17).
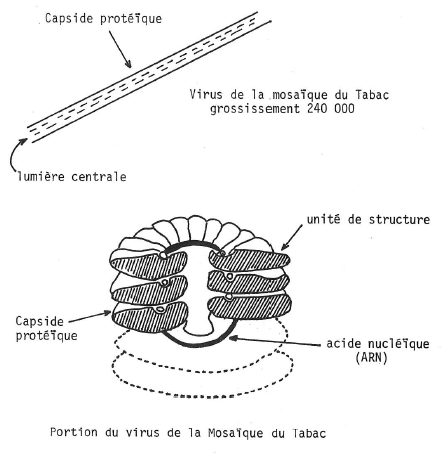
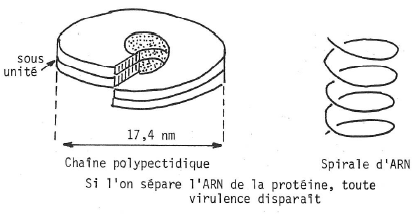
Fig. 17.
La mosaïque du Tabac mérite une attention particulière, c’est la plus ancienne des maladies virales qui s’attaquent aux plantes qui a été très étudiée.
En 1935, Stanley, aux États-Unis, réussissait à précipiter sous forme d’aiguilles microscopiques, cristallines, ayant une symétrie à deux dimensions, des solutions purifiées et concentrées, des virus de la mosaïque du Tabac.
Ce résultat fit grand bruit à l’époque car l’on avait cru que le virus allait combler le hiatus, si hiatus il y a, séparant la matière vivante de la matière inerte.
D’autres virus cristallisèrent à leur tour sous forme de cristaux à facettes, proches de la symétrie à trois dimensions.
De toute évidence, la cristallisation des virus apporte un argument de poids aux tenants de la nature non vivante des virus.
L’étude au microscope électronique a permis de définir la structure du virus de la mosaïque du Tabac :
L’acide nucléique (ARN dans ce cas) une structure tubulaire sous forme d’un cylindre creux de 4nm de rayon. Autour s’articulent et s’enroulent en spirale continue les sous-unités protidiques. L’ensemble forme une baguette creuse, de structure hélicoïdale, longue de 30nm et d’un diamètre de 17,4nm.
Les sous-unités protéiques sont disposées en hélice dont le pas est de 2,3nm. Chaque tour d’hélice comprend 16 sous-unités 1/3 et le virus au total 2200 sous-unités protéiques sur une longueur de 300 nm.
ANNEXE II
Pour un peu de clarté (fig. 18).
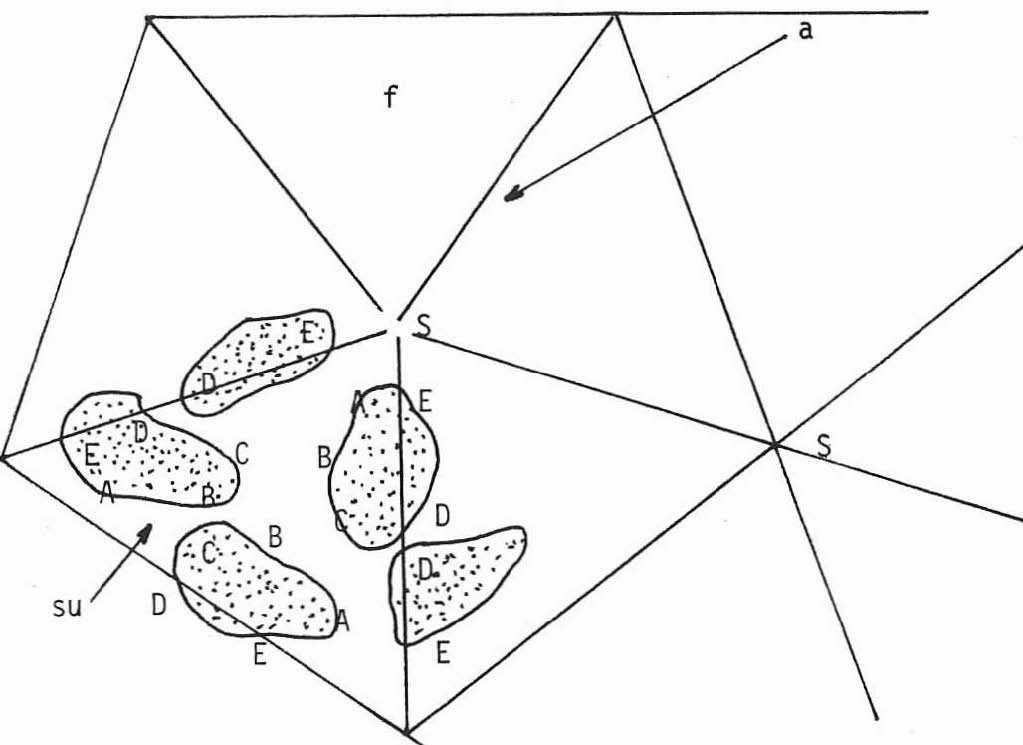
S = sommet, f = face, a = arête, su = sous-unité
Fig. 18. Une portion de la surface de la capside.
Un des 12 sommets de l’icosaèdre où se rencontrent 3 triangles équilatéraux et 5 arêtes.
Au total, 30 arêtes (a) et 20 faces (f).
Sur chaque face nous avons représenté 3 sous-unités (su), soit 60 pour l’ensemble de l’icosaèdre.
La morphologie d’un virus est, dans le détail, variable suivant les espèces ; la disposition générale reste cependant uniforme.
On distinguer deux parties :
- une interne représente le matériel génétique formé selon les espèces, sous la forme de la double hélice.
- soit d’acide désoxyribonucléique (ADN),
- soit d’acide ribonucléique (ARN), cas du virus de la mosaïque du Tabac.
- une externe : la capside qui renferme un petit nombre d’espèces moléculaires, de nature protéique.
Ces molécules constituent alors des sous-unités, ou capsomères qui sont disposées les unes par rapport aux autres dans un arrangement géométrique régulier (nous avons cité l’isocaèdre).
Le virus a dès lors une forme polyédrique qui permet éventuellement, par agrégation d’un grand nombre de particules, de donner naissance à de véritables cristaux de dimensions macroscopiques.
Découvrez + de 1100 textes des conférences du CDI sur le site du CDI de Garches
Vos commentaires et vos conseils contribuent à l’amélioration de nos parutions.
Vous disposez de l’espace « COMMENTAIRES » ci-dessous pour les exprimer.
Merci et à bientôt pour votre prochaine visite.

Laisser un commentaire